题目内容
【题目】某品牌洁厕灵的成分是硫酸与盐酸的混合溶液。某课外活动小组想测定20g该品牌洁厕灵溶液中H2SO4和HCl的质量。取20g该品牌的洁厕灵溶液于烧杯中,不断滴加溶质质量分数为17.1%的氢氧化钡溶液,反应过程中烧杯中产生沉淀质量和烧杯中溶液pH变化的部分数据如下所示:
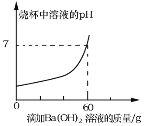
滴加氢氧化钡溶液的质量/g | 5 | 10 | 25 |
烧杯中产生沉淀的质量/g | 1.165 | 2.33 | 4.66 |
(已知BaCl2溶液的pH = 7;Ba的相对原子质量137)
求:20g该品牌洁厕灵溶液中H2SO4的质量和HCl的质量。
【答案】解:由题意可知:H2SO4完全反应后产生BaSO4沉淀的质量是4.66g。
设20g该品牌洁厕灵溶液中H2SO4的质量为x。
Ba(OH)2+ H2SO4 = BaSO4+ 2H2O
98 233
x 4.66g
98/233=x/4.66g
x=1.96g
由题意可知:与HCl完全反应的Ba(OH)2溶液的质量为:
60g-20g=40g
设20g该品牌洁厕灵溶液中HCl的质量为y。
Ba(OH)2+ 2HCl= BaCl2+ 2H2O
171 73
40g×17.1﹪ y
171/73=(40g×17.1﹪)/y
y=2.92g
答:设20g该品牌洁厕灵溶液中H2SO4的质量为1.96g,HCl的质量为2.92g。
【解析】由题意可知:H2SO4完全反应后产生BaSO4沉淀的质量是4.66g,设20g该品牌洁厕灵溶液中H2SO4的质量为x。
Ba(OH)2+ H2SO4 = BaSO4+ 2H2O
98 233
x 4.66g
98/233=x/4.66g
x=1.96g
再由题意可知:与HCl完全反应的Ba(OH)2溶液的质量为:
60g-20g=40g
设20g该品牌洁厕灵溶液中HCl的质量为y。
Ba(OH)2+ 2HCl= BaCl2+ 2H2O
171 73
40g×17.1﹪ y
171/73=(40g×17.1﹪)/y
y=2.92g
计算得知20g该品牌洁厕灵溶液中H2SO4的质量为1.96g,HCl的质量为2.92g

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
