题目内容
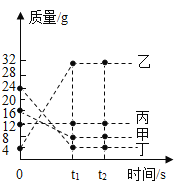
【题目】下列图像能正确体现对应关系的是
A.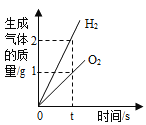 实验室采用直流电来电解水
实验室采用直流电来电解水
B. 等质量的镁粉和铝粉加入足量的稀盐酸
等质量的镁粉和铝粉加入足量的稀盐酸
C.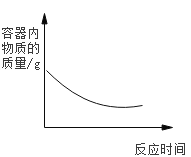 铁丝在盛有氧气的密闭容器中燃烧
铁丝在盛有氧气的密闭容器中燃烧
D.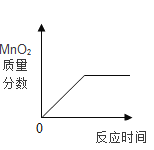 加热一定量氯酸钾和二氧化锰的混合物
加热一定量氯酸钾和二氧化锰的混合物
【答案】B
【解析】
A、在电解水实验中,水通电生成氢气和氧气,氢气与氧气的体积比为2:1,图象显示的是氢气与氧气的质量比为2:1,不符合题意;
B、设镁、铝的质量为M,产生氢气质量分别为X、Y。
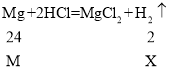
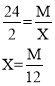
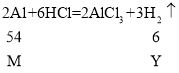

因为![]() , 所以铝产生的氢气比镁的多,铝的曲线要比镁的高,但镁的活动性比铝的强,反应所需时间要短,符合题意;
, 所以铝产生的氢气比镁的多,铝的曲线要比镁的高,但镁的活动性比铝的强,反应所需时间要短,符合题意;
C、根据质量守恒定律,铁丝在盛有氧气的密闭容器中燃烧,物质的总质量不变,不符合题意;
D、一定量氯酸钾和二氧化锰的混合物中,二氧化锰的质量分数不可能为0,所以曲线起点不能从0点起,不符合题意。故选B。

 阅读快车系列答案
阅读快车系列答案【题目】小花同学从家乡的山上带回了一些石灰石样品,同学们利用这些石灰石样品做了如下实验:取样品20g放入烧杯中,将10g稀盐酸分5次加入,实验过程所得的数据如表所示(已知石灰石样品中的杂质不参与反应,也不溶于水)。根据实验数据计算:
实验次数 | 数加入稀盐酸的质量/g | 剩余固体的质量/g |
1 | 20 | 16 |
2 | 20 | 12 |
3 | 20 | 8 |
4 | 20 | 5 |
5 | 20 | 5 |
(1)盐酸在加到第_____次开始过量;
(2)石灰石样品中CaCO3的质量分数=_____;
(3)所用稀盐酸中溶质的质量分数_____(写出计算过程,结果精确到0.1%)。
【题目】为了测定液化气中丙烷(C3H8)在氧气不足时的燃烧产物,将一定量的丙烷和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表:
物质 | 丙烷 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 4.4 | 12.8 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 7.2 | 4.4 | a |
下列判断不正确的是( )
A.表中a的值为5.6
B.此反应不属于反应的基本类型
C.X一定不含氢元素
D.X只含碳元素