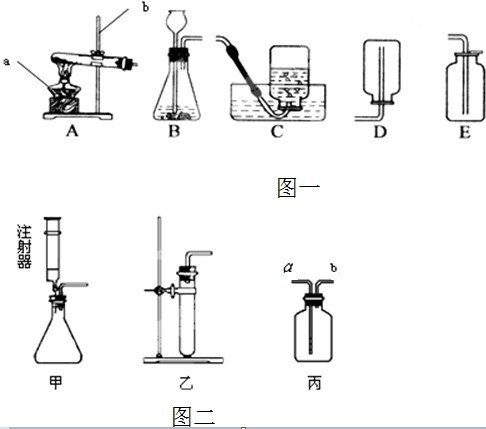
题目内容
实验室用氯酸钾与二氧化锰混合加热制取氧气。取它们的混合物14.25 g加热,完全反应后,冷却称量,得到剩余固体的质量为9.45 g。试计算:
⑴ 生成氧气的质量。 ⑵ 原混合物中氯酸钾的质量(写出计算过程)。
⑴4.8 g ⑵12.25 g
解析试题分析:⑴氯酸钾在二氧化锰作催化剂的作用下,受热分解为氯化钾和氧气,由于氧气的逸出,故反应后的固体质量会减小,根据质量守恒定律可知,减少的质量即为生成氧气的质量,故生成氧气的质量=14.25g-9.45g=4.8g
⑵根据题意书写反应的化学方程式,利用生成的氧气的质量,结合方程式中氯酸钾与氧气的质量比,可求出完全反应的氯酸钾的质量。
解:设原混合物中氯酸钾的质量至少为x,
2KClO3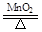 2KCl+3O2↑
2KCl+3O2↑
245 96
x 4.8g
245:96= x:4.8g
解得x=12.25g
答:⑴生成氧气的质量为4.8g;⑵原混合物中氯酸钾的质量为12.25g。
考点:根据化学反应方程式的计算
点评:解答本题的关键是根据题意,利用质量守恒定律找出恰好完全反应时,生成的氧气的质量,再利用相关的化学反应书写化学方程式,并依据已知量对未知的应求量进行求解计算即可。

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目