题目内容
上海世博会上需要很多的钢材来作为建筑材料,某中学的初三学生在一次社会实践活动中,为了检验所用钢材是否合格,他们到钢材下料场的电锯下获取一包钢材粉末样品.回到实验室,同学们进行了分组实验,实验数据记录如下表,请认真阅读上面的内容,分析所有数据,回答下列问题:(钢的含碳量:0.03%~2%烧杯的质量为25.4g,计算结果精确到0.1%)| 第一组 | 第二组 | 第三组 | |
| 烧杯+稀硫酸 | 200g | 150g | 150g |
| 加入的铁样品 | 8.5g | 8.5g | 13.5g |
| 充分反应后,烧杯+剩余物 | 208.2g | 158.2g | 163.2g |
(2)假设杂质全部为碳,请通过计算说明这批钢材是否合格?
(3)试计算恰好完全反应后所得溶液中溶质的质量分数?
【答案】分析:(1)首先分析第一组和第二组产生的氢气量相同,铁样品质量相同,但第一组中硫酸质量多,说明第一组硫酸过量;在分析第二组和第三组硫酸质量相同,铁样品质量第三组多,而产生的氢气量仍相同,说明第三组铁样品过量.综上分析,所以第二组中铁样品和稀硫酸恰好完全反应.
(2)上面分析已经知道,第二组是恰好完全反应的,所以计算时要用第二组的数据,利用氢气质量得到铁的质量,然后得到铁样品中杂质碳的质量.
(3)用第二组的数据,利用氢气质量得到硫酸亚铁的质量,进而得到硫酸亚铁的质量分数.
解答:解:(1)由以上第一组和第二组分析可知,8.5g铁样品能产生0.3g氢气,第二组和第三组分析可知,124.6g稀硫酸能产生0.3g氢气,所以8.5g铁样品和124.6g稀硫酸能恰好完全反应,即为第二组.
(2)设样品中铁的质量为x,
生成氢气的质量为:150g+8.5g-158.2g=0.3g
Fe+H2SO4═FeSO4+H2↑
56 152 2
x y 0.3 g
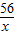 =
=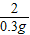
x=8.4g
8.5g铁样品中碳的质量为8.5g-8.4g=0.1g
该钢的含碳量为: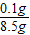 ×100%=1.2%
×100%=1.2%
因为:0.03%<1.2%<2%,所以钢材合格
(3)设生成硫酸亚铁的质量为y,
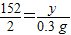
y=22.8g
8.5g铁样品和稀硫酸能恰好完全反应后溶液的质量为:158.2g-25.4g-0.1g=132.7g
溶液中溶质的质量分数为: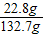 ×100%=17.2%
×100%=17.2%
答:(1)二
(2)这批钢材合格.
(3)恰好完全反应后所得溶液中溶质的质量分数为17.2%.
点评:此题是一道表格数据型的计算题,而且表格中给出的是多组数据,所以此题的关键是通过观察、分析和比较全部数据,找出有用数据来进行解题.此题很好的考查了学生发散思维的能力.
(2)上面分析已经知道,第二组是恰好完全反应的,所以计算时要用第二组的数据,利用氢气质量得到铁的质量,然后得到铁样品中杂质碳的质量.
(3)用第二组的数据,利用氢气质量得到硫酸亚铁的质量,进而得到硫酸亚铁的质量分数.
解答:解:(1)由以上第一组和第二组分析可知,8.5g铁样品能产生0.3g氢气,第二组和第三组分析可知,124.6g稀硫酸能产生0.3g氢气,所以8.5g铁样品和124.6g稀硫酸能恰好完全反应,即为第二组.
(2)设样品中铁的质量为x,
生成氢气的质量为:150g+8.5g-158.2g=0.3g
Fe+H2SO4═FeSO4+H2↑
56 152 2
x y 0.3 g
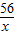 =
=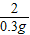
x=8.4g
8.5g铁样品中碳的质量为8.5g-8.4g=0.1g
该钢的含碳量为:
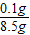 ×100%=1.2%
×100%=1.2%因为:0.03%<1.2%<2%,所以钢材合格
(3)设生成硫酸亚铁的质量为y,
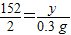
y=22.8g
8.5g铁样品和稀硫酸能恰好完全反应后溶液的质量为:158.2g-25.4g-0.1g=132.7g
溶液中溶质的质量分数为:
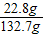 ×100%=17.2%
×100%=17.2%答:(1)二
(2)这批钢材合格.
(3)恰好完全反应后所得溶液中溶质的质量分数为17.2%.
点评:此题是一道表格数据型的计算题,而且表格中给出的是多组数据,所以此题的关键是通过观察、分析和比较全部数据,找出有用数据来进行解题.此题很好的考查了学生发散思维的能力.

练习册系列答案
相关题目
上海世博会上需要很多的钢材来作为建筑材料,某中学的初三学生在一次社会实践活动中,为了检验所用钢材是否合格,他们到钢材下料场的电锯下获取一包钢材粉末样品.回到实验室,同学们进行了分组实验,实验数据记录如下表,请认真阅读上面的内容,分析所有数据,回答下列问题:(钢的含碳量:0.03%~2%烧杯的质量为25.4g,计算结果精确到0.1%)
(1)第 组所取的铁样品和稀硫酸恰好完全反应.
(2)假设杂质全部为碳,请通过计算说明这批钢材是否合格?
(3)试计算恰好完全反应后所得溶液中溶质的质量分数?
| 第一组 | 第二组 | 第三组 | |
| 烧杯+稀硫酸 | 200g | 150g | 150g |
| 加入的铁样品 | 8.5g | 8.5g | 13.5g |
| 充分反应后,烧杯+剩余物 | 208.2g | 158.2g | 163.2g |
(2)假设杂质全部为碳,请通过计算说明这批钢材是否合格?
(3)试计算恰好完全反应后所得溶液中溶质的质量分数?
上海世博会上需要很多的钢材来作为建筑材料,某中学的初三学生在一次社会实践活动中,为了检验所用钢材是否合格,他们到钢材下料场的电锯下获取一包钢材粉末样品.回到实验室,同学们进行了分组实验,实验数据记录如下表,请认真阅读上面的内容,分析所有数据,回答下列问题:(钢的含碳量:0.03%~2%烧杯的质量为25.4g,计算结果精确到0.1%)
(1)第______组所取的铁样品和稀硫酸恰好完全反应.
(2)假设杂质全部为碳,请通过计算说明这批钢材是否合格?
(3)试计算恰好完全反应后所得溶液中溶质的质量分数?
| 第一组 | 第二组 | 第三组 | |
| 烧杯+稀硫酸 | 200g | 150g | 150g |
| 加入的铁样品 | 8.5g | 8.5g | 13.5g |
| 充分反应后,烧杯+剩余物 | 208.2g | 158.2g | 163.2g |
(2)假设杂质全部为碳,请通过计算说明这批钢材是否合格?
(3)试计算恰好完全反应后所得溶液中溶质的质量分数?
