题目内容
诺贝尔化学奖的成果与一种新的化学合成方法有关.新的合成过程更简单快捷,产生的副产品和有害废物更少,原子利用率更高,是“绿色化学”的典范.下列反应中,符合以上“绿色化学”概念是( )
A、烧制生石灰:CaCO3
| ||||
| B、利用纯碱制碳酸氢钠:Na2CO3+CO2+H2O=2NaHCO3 | ||||
| C、制氢氧化铜:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 | ||||
| D、湿法炼铜:Fe+CuSO4=FeSO4+Cu |
考点:绿色化学
专题:化学与环境保护
分析:传统的化学工业给环境带来的污染十分严重,有识之士提出了绿色化学的号召,它的主要特点之一是:提高原子的利用率,使原料中的所有的原子全部转化到产品中,实现“零排放”,即所要的反应生成物中,若反应物里的原子数百分之百都得到了利用,那么,这个化学反应就没有废弃物产生.在我们所学的反应类型中,化合反应符合了这一特点,它能把反应物的各种原子都集中到同一生成物中,没有副产品产生,也就不会产生污染.
解答:解:符合绿色化学这一特点的反应类型是化合反应.化合反应的特点是多合一,生成物只有一种.
A、烧制生石灰的反应是分解反应;故A不正确;
B、利用纯碱制碳酸氢钠的化学反应属于化合反应.故B正确;
C、制氢氧化铜的化学反应属于复分解反应;故C不正确;
D、湿法炼铜的化学反应是置换反应;故D不正确.
故选B.
A、烧制生石灰的反应是分解反应;故A不正确;
B、利用纯碱制碳酸氢钠的化学反应属于化合反应.故B正确;
C、制氢氧化铜的化学反应属于复分解反应;故C不正确;
D、湿法炼铜的化学反应是置换反应;故D不正确.
故选B.
点评:本题考查了绿色化学的主要特点,原理就是要从源头消除污染.通过试题,培养了学生的环保意识,此类考题与环境保护有关,是热门考点.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
下列实验操作正确的( )
A、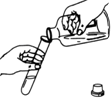 |
B、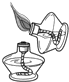 |
C、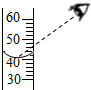 |
D、 |
6月5日是“世界环境保护日”,2009年我国的宣传口号是“减少污染,行动起来”.某化学研究小组提出如下四条设想,你认为其中合理可行的是( )
| A、在燃煤中加入固硫剂,以减少“酸雨”的形成 |
| B、大力开发水能、太阳能等清洁能源,禁止使用化石燃料 |
| C、废弃塑料可采用焚烧的方法处理,以解决“白色污染” |
| D、废干电池实施掩埋处理以防止对水源和土壤的污染 |
下列叙述符合实验事实的是( )
| A、久置于空气中的熟石灰,加入稀盐酸会有气体放出 |
| B、氢氧化钠与硝酸钡能发生反应 |
| C、通入CO2后的石蕊溶液变红,所以CO2是酸 |
| D、工业用盐(NaNO2)也是盐,用它腌制的泡菜可以放心食用 |
能一次鉴别Ca(OH)2、稀HCl、NaCl三种无色溶液的试剂是( )
| A、Na2CO3溶液 |
| B、BaCl2溶液 |
| C、酚酞 |
| D、硝酸 |
下列实验基本操作中,正确的是( )
| A、用嘴吹灭酒精灯的火焰 |
| B、用嘴吹灭蜡烛的火焰 |
| C、用燃着的酒精灯火焰点燃另一盏酒精灯 |
| D、用燃着的蜡烛火焰点燃另一支蜡烛 |
化学变化伴随能量变化.某同学对碳酸钠、碳酸氢钠与盐酸反应过程中的放、吸热情况进行探究.步骤为:①向试剂1中加入试剂2,搅拌、测温;②再加入试剂3,搅拌、测温.记录数据如下:
则下列说法中,不正确的是( )
| 试剂1 | 试剂2 温度/℃ | 溶解后温度/℃ | 静置后温度/℃ | 试剂3 温度/℃ | 混合后温度/℃ |
| 0.5gNa2CO3 | 10mL H2O 20.0 | 23.3 | 20.0 | 10mL HCl(20%) 20.0 | 23.7 |
| 0.5gNaHCO3 | 10mL H2O 20.0 | 18.5 | 20.0 | 10mL HCl(20%) 20.0 | 20.8 |
| A、物质溶于水的过程也有吸热、放热现象 |
| B、若无步骤②,同样可以达到目的 |
| C、碳酸钠与盐酸反应放出的热量一定比碳酸氢钠反应放出的多 |
| D、若将实验中所用盐酸换成相同浓度的稀硫酸对实验结论没有影响 |