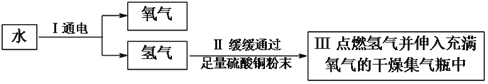题目内容
【题目】某溶液可能含有HCl、H2SO4、NaNO3、CuCl2中的一种或几种,为了探究其组成,向一定质量的该溶液中逐滴加入Ba(OH)2溶液,生成沉淀的质量与所加Ba(OH)2溶液的质量之间的关系如图所示。
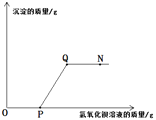
(1)O至P段发生反应的化学方程式为_________。
(2)P至Q段产生的沉淀物是__________。
(3)Q点时,所得溶液的pH___7(填“>”“<”或“=”)。
(4)N点时,溶液中一定含有的溶质是_______,可能含有的溶质是_______。
【答案】 2HCl + Ba(OH)2 = BaCl2 + 2H2O Cu(OH)2 = BaCl2和Ba(OH)2 NaNO3
【解析】(1)OP段加入氢氧化钡后没有沉淀生成,说明氢氧化钡与溶液中的酸发生中和反应,该酸只能是稀盐酸,不可能是稀硫酸,因为稀硫酸与氢氧化钡反应有白色的沉淀生成,也能说明溶液中没有硫酸根离子,氢氧化钡与稀盐酸反应生成氯化钡和水,反应方程式为2HCl + Ba(OH)2 = BaCl2 + 2H2O
(2)由题可知,PQ段是氢氧化钡与氯化铜的反应,故生成的沉淀是氢氧化铜;
(3)Q点时,氢氧化钡与氯化铜恰好完全反应,故溶液的Ph=7;
(4)N点时,溶液中含有过剩的氢氧化钡,OP段、PQ段反应生成的氯化钡,故溶质是氢氧化钡和氯化钡,可能含有的溶质是硝酸钠;

 阅读快车系列答案
阅读快车系列答案【题目】工业铁红主要成分是Fe2O3,还含有少量的FeO、Fe3O4
【查阅资料】(1)草酸晶体(H2C2O43H2O)在浓硫酸作用下受热分解,化学方程式为:H2C2O43H2O ![]() CO2↑+CO↑+H2O
CO2↑+CO↑+H2O
(2)碱石灰是固体NaOH和CaO的混合物,能吸收水蒸气和二氧化碳。
(3)铁的常见氧化物中铁的质量分数:
铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
铁的质量分数 | 77.8% | 70.0% | 72.4% |
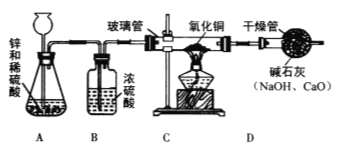
【问题讨论】为了测定铁红中铁的质量分数,小组间进行如下实验。(装置气密性良好)
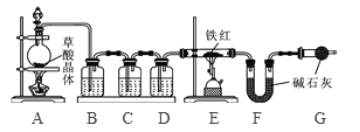
(1)该实验为了保证进入E中的气体是纯净、干燥的CO,则B、C、D中的试剂依次是________(填字母序号)
a.浓硫酸 b.澄清的石灰水 c氢氧化钠溶液
(2)C装置的作用是 __________________________。
(3)写出E装置中所发生反应的一个化学方程式: _____________________。
(4)称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数。
①若E中充分反应后得到铁粉的质量为mg,则 ____ < m < ______。
②若实验前后称得F装置増重7.7g,则此铁红中铁的质量分数是 _________。
【实验反思】 (1)如果缺少G装置(不考虑其他因素),则测得样品中铁的质量分数会 ________(选填“偏小”“不变”“偏大”)。
(2)该实验装置的一个明显缺陷是 ___________________。
【题目】下表是NaCl和KNO3在不同温度时的溶解度,回答问题。
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 | |
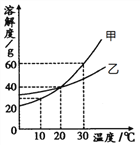
(1)两种物质中,溶解度受温度影响变化较大的是_________。
(2)60℃时,按图示操作:
![]()
A中溶质是_____(填“饱和”或“不饱和”)溶液,C中溶液的总质量是______g。
(3)50℃时,将两种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到50℃,剩余溶液的质量:NaCl溶液_____(填“大于”“等于”或“小于”) KNO3溶液。