题目内容
将5g一氧化碳和二氧化碳的混合气体先缓缓通过足量的灼热氧化铜后,再缓缓通入足量的澄清石灰水中,得到白色沉淀15g(假设每步反应都进行完全),则原混合气体中一氧化碳的质量分数为
- A.12%
- B.44%
- C.56%
- D.88%
C
分析:由气体通到足量的澄清石灰水中得到白色沉淀15g可知碳酸钙的质量为15g,然后利用化学反应计算出还原氧化铜后的二氧化碳的质量,再利用碳元素的质量守恒来计算一氧化碳的质量,最后计算原混合气体中一氧化碳的质量分数.
解答:由题意知碳酸钙的质量为15g,设与石灰水反应的二氧化碳的质量为x,
则CO2+Ca(OH)2═CaCO3↓+H2O
44 100
x 15g
 ,解得x=6.6g,
,解得x=6.6g,
设原混合物中的一氧化碳的质量为y,则反应前的二氧化碳为5g-y
则一氧化碳中的碳元素的质量等于y×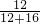 ×100%
×100%
反应前混合物中中二氧化碳中碳元素的质量等于(5g-y)×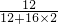 ×100%
×100%
而反应后二氧化碳中碳元素的质量为6.6g×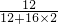 ×100%
×100%
由于反应前后由碳元素的质量守恒可知,
y×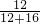 ×100%+(5g-y)×
×100%+(5g-y)×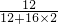 ×100%=6.6g×
×100%=6.6g×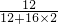 ×100%,
×100%,
解得y=2.8g,
则原混合气体中一氧化碳的质量分数为 ×100%=56%,
×100%=56%,
故选C.
点评:本题考查学生利用化学反应方程式及元素守恒的方法来计算混合物中物质的质量分数,注意习题中每步反应都进行完全则可利用元素守恒来分析解答.
分析:由气体通到足量的澄清石灰水中得到白色沉淀15g可知碳酸钙的质量为15g,然后利用化学反应计算出还原氧化铜后的二氧化碳的质量,再利用碳元素的质量守恒来计算一氧化碳的质量,最后计算原混合气体中一氧化碳的质量分数.
解答:由题意知碳酸钙的质量为15g,设与石灰水反应的二氧化碳的质量为x,
则CO2+Ca(OH)2═CaCO3↓+H2O
44 100
x 15g
 ,解得x=6.6g,
,解得x=6.6g,设原混合物中的一氧化碳的质量为y,则反应前的二氧化碳为5g-y
则一氧化碳中的碳元素的质量等于y×
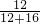 ×100%
×100%反应前混合物中中二氧化碳中碳元素的质量等于(5g-y)×
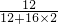 ×100%
×100%而反应后二氧化碳中碳元素的质量为6.6g×
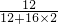 ×100%
×100%由于反应前后由碳元素的质量守恒可知,
y×
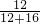 ×100%+(5g-y)×
×100%+(5g-y)×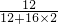 ×100%=6.6g×
×100%=6.6g×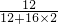 ×100%,
×100%,解得y=2.8g,
则原混合气体中一氧化碳的质量分数为
 ×100%=56%,
×100%=56%,故选C.
点评:本题考查学生利用化学反应方程式及元素守恒的方法来计算混合物中物质的质量分数,注意习题中每步反应都进行完全则可利用元素守恒来分析解答.

练习册系列答案
相关题目
 是,下列说法不正确的是
是,下列说法不正确的是