题目内容
【题目】有一种石灰石样品的成分是CaCO3和SiO2(已知SiO2既不溶于水也不与盐酸反应)。现取8g石灰石样品与50g足量的稀盐酸完全反应后,称得容器内物质的总质量为55.36g.试回答下列问题:
(1)反应产生二氧化碳的质量为_____.
(2)该石灰石样品中碳酸钙的质量分数是多少?_____
【答案】2.64g 75%
【解析】
本题考查的是有关化学方程式的混合物计算,用一种成分为CaCO3和SiO2石灰石样品与盐酸反应,测量样品中碳酸钙的质量分数。
(1)根据质量守恒定律,反应产生二氧化碳的质量为![]()
(2)解:该石灰石样品中碳酸钙的质量为X,
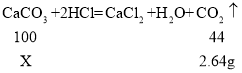
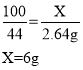
该石灰石样品中碳酸钙的质量分数是:![]()
答:该石灰石样品中碳酸钙的质量分数是75%。

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
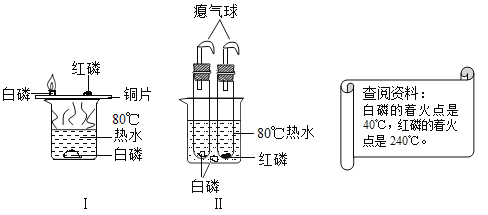
【题目】某实验小组用如图实验方法来探究燃烧的条件。
实验二 |
|
(1)按装置I进行实验,观察实验现象,红磷不能燃烧是因为_____,水中白磷不能燃烧,若欲使水中白磷出现燃烧的奇观,可采取的方法是_____。
(2)改进后的装置Ⅱ与装置相比,其优点是_____。
(3)“水火不相容”是指水能灭火,其实水有时也可以“生火”。比如用脱脂棉包裹好过氧化钠(Na2O2),往棉球上滴水即可看到“滴水生火”的奇观,因为过氧化钠遇到水生成NaOH和另一种物质,写出其反应的符号表达式为_____(不要求配平),该反应是_____(填“吸热”或“放热”)反应。