题目内容
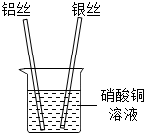 (2013?南岗区一模)张南同学为了验证铝、铜、银的金属活动性顺序,设计了如下实验方案:将铝丝、银丝分别插入到硝酸铜溶液中,如图,根据实验现象可以判断出三种金属的金属活动性强弱顺序.请回答下列问题.
(2013?南岗区一模)张南同学为了验证铝、铜、银的金属活动性顺序,设计了如下实验方案:将铝丝、银丝分别插入到硝酸铜溶液中,如图,根据实验现象可以判断出三种金属的金属活动性强弱顺序.请回答下列问题.(1)判断铝的活动性比铜强的现象是
铝的表面附着一层红色的固体
铝的表面附着一层红色的固体
;若没有观察到预期现象,其原因是铝没有除锈,表面有一层致密的保护膜
铝没有除锈,表面有一层致密的保护膜
(不考虑硝酸铜溶液).(2)上述实验中发生反应的化学方程式为
2Al+3Cu(NO3)2=2Al(NO3)3+3Cu
2Al+3Cu(NO3)2=2Al(NO3)3+3Cu
;由此实验得出三种金属的活动性顺序为铝>铜>银
铝>铜>银
.分析:根据在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来分析现象及结论.
解答:解:(1)铝的活动性比铜强,因此会置换出硫酸铜中的铜,现象为:铝的表面附着一层红色的固体;若铝没有除锈,表面有一层致密的保护膜,就不会和硫酸铜发生反应,因此观察不到预期现象;
(2)铝与硝酸铜反应生成硝酸铝和铜,反应的化学方程式为:2Al+3Cu(NO3)2=2Al(NO3)3+3Cu;由于在银的表面不会出现一层红色的固体,说明银的活动性比铜弱,因此三种金属的活动性顺序为:铝>铜>银;
故答案为:(1)铝的表面附着一层红色的固体;铝没有除锈,表面有一层致密的保护膜;(2)2Al+3Cu(NO3)2=2Al(NO3)3+3Cu;铝>铜>银.
(2)铝与硝酸铜反应生成硝酸铝和铜,反应的化学方程式为:2Al+3Cu(NO3)2=2Al(NO3)3+3Cu;由于在银的表面不会出现一层红色的固体,说明银的活动性比铜弱,因此三种金属的活动性顺序为:铝>铜>银;
故答案为:(1)铝的表面附着一层红色的固体;铝没有除锈,表面有一层致密的保护膜;(2)2Al+3Cu(NO3)2=2Al(NO3)3+3Cu;铝>铜>银.
点评:本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行分析,还要注意化学方程式的书写.

练习册系列答案
相关题目