题目内容
【题目】从海水中制备纯碱和金属镁的流程如图所示: 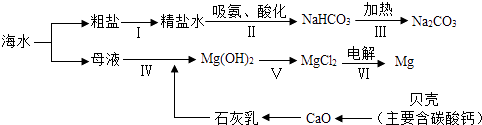
下列说法不正确的是( )
A.步骤Ⅱ中吸氨的作用是使溶液呈碱性,促进二氧化碳吸收
B.第Ⅲ歩反应的化学方程式是2NaHCO3 ![]() Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
C.步骤Ⅳ发生的是置换反应
D.步骤Ⅴ中所加试剂是盐酸
【答案】C
【解析】解:A、氨气是碱性气体,在酸性溶液的吸收效果好,故A正确; B、第Ⅲ歩的反应是碳酸氢钠在加热的条件下生成碳酸钠、水和二氧化碳,化学方程式是:2NaHCO3 ![]() Na2CO3+CO2↑+H2O,故B正确;
Na2CO3+CO2↑+H2O,故B正确;
C、步骤Ⅳ发生的反应是熔融状态的氯化镁在通电的条件下生成镁和氯气,属于分解反应,故C错误;
D、步骤Ⅴ分数的反应是氢氧化镁和盐酸反应生成氯化镁和水,所以所加试剂是盐酸,故D正确.
故选:C.
A、根据氨气是碱性气体,在酸性溶液的吸收效果好进行分析;
B、根据第Ⅲ歩的反应是碳酸氢钠在加热的条件下生成碳酸钠、水和二氧化碳进行分析;
C、根据步骤Ⅳ发生的反应是熔融状态的氯化镁在通电的条件下生成镁和氯气进行分析;
D、根据步骤Ⅴ分数的反应是氢氧化镁和盐酸反应生成氯化镁和水进行分析.

练习册系列答案
相关题目