题目内容
(2012?兰州)下列装置常用于实验室制取气体.根据给出的装置回答下列问题:
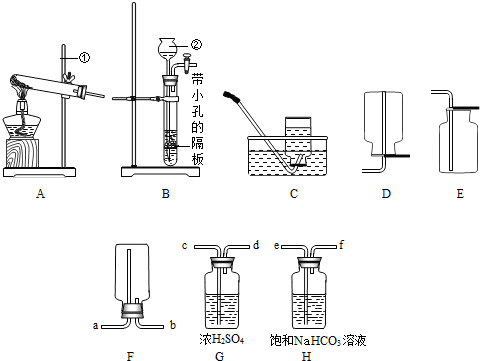
(1)指出编号仪器名称:①
(2)实验室利用A装置制取氧气,反应原理用化学方程式表示为
(3)制取并收集二氧化碳应选择的装置是
(4)将纯净的二氧化碳气体通入盛有蒸馏水的洗气瓶一段时间后,测得该装置中溶液的pH

(1)指出编号仪器名称:①
铁架台
铁架台
;②长颈漏斗
长颈漏斗
.(2)实验室利用A装置制取氧气,反应原理用化学方程式表示为
2KClO3
2KCl+3O2↑
| ||
| △ |
2KClO3
2KCl+3O2↑
.利用C装置收集氧气的最佳时刻是
| ||
| △ |
导管口有气泡连续均匀冒出时
导管口有气泡连续均匀冒出时
.用收集到的氧气完成硫粉燃烧实验后,还需向集气瓶内加入适量氢氧化钠溶液,目的是2NaOH+SO2=Na2SO3+H2O
2NaOH+SO2=Na2SO3+H2O
(用化学方程式表示).(3)制取并收集二氧化碳应选择的装置是
BE
BE
(从A--E中选择),使用该套装置制取气体的突出优点是可以随时控制反应发生或停止,
可以随时控制反应发生或停止,
,该反应原理用化学方程式表示为CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
.若改用F装置收集二氧化碳,则气体应从b
b
端进入.制得的二氧化碳中常含有少量的氯化氢气体与水蒸气,欲使个G、H装置将以上杂质气体除去,则装置正确的连接顺序是:混合气体→efcd
efcd
(用端口字母表示).(4)将纯净的二氧化碳气体通入盛有蒸馏水的洗气瓶一段时间后,测得该装置中溶液的pH
<
<
(填“>”、“<”或“=”)7,对该现象的合理解释为H2O+CO2=H2CO3
H2O+CO2=H2CO3
(用化学方程式表示).分析:(1)熟悉常见仪器的名称和用途;
(2)分析装置的特点,选择药品制取氧气.根据制取氧气的步骤及注意的事项,把握开始收集的时机.根据二氧化硫的是一种有污染的气体及性质分析向集气瓶内加入适量氢氧化钠溶液的目的,写出反应的方程式;
(3)根据实验室制取二氧化碳的反应物的状态和反应条件确定发生装置;根据二氧化碳的收集方法选择收集装置.分析该装置的优点,写出反应的方程式.根据二氧化碳的密度与空气的密度的关系分析用F装置收集二氧化碳的进气端.当二氧化碳中含有少量的氯化氢气体与水蒸气时,应先除去氯化氢气体再除去水蒸气,分析连接装置的顺序;
(4)根据二氧化碳与水反应的性质进行分析.
(2)分析装置的特点,选择药品制取氧气.根据制取氧气的步骤及注意的事项,把握开始收集的时机.根据二氧化硫的是一种有污染的气体及性质分析向集气瓶内加入适量氢氧化钠溶液的目的,写出反应的方程式;
(3)根据实验室制取二氧化碳的反应物的状态和反应条件确定发生装置;根据二氧化碳的收集方法选择收集装置.分析该装置的优点,写出反应的方程式.根据二氧化碳的密度与空气的密度的关系分析用F装置收集二氧化碳的进气端.当二氧化碳中含有少量的氯化氢气体与水蒸气时,应先除去氯化氢气体再除去水蒸气,分析连接装置的顺序;
(4)根据二氧化碳与水反应的性质进行分析.
解答:解:(1)由图示可知标号仪器①是铁架台,②是长颈漏斗;
(2)由A装置可知,此装置是加热固体制取气体的装置,如制取氧气,可用加热氯酸钾和二氧化锰混合物的方法,反应的方程式是:2KClO3
2KCl+3O2↑;利用排水法收集氧气的最佳时刻是导管口有气泡连续均匀冒出时;二氧化硫是一种有害的气体,利用能与氢氧化钠反应的性质将其吸收掉,反应的方程式是:2NaOH+SO2=Na2SO3+H2O;
(3)实验室用大理石和稀盐酸反应制取二氧化碳,反应物的状是固体和液体,反应条件是常温,应选用发生装置B,由于二氧化碳的密度大于空气的密度,可选用收集装置E;使用该套装置制取气体的突出优点是:可以随时控制反应发生或停止,该反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;若改用F装置收集二氧化碳,由于二氧化碳的密度大于空气的密度,则气体应从b 端进入.制得的二氧化碳中常含有少量的氯化氢气体与水蒸气,要将以上杂质气体除去,应先将氯化氢气体除去,在除去水蒸气.则装置正确的连接顺序是:混合气体→efcd;
(4)二氧化碳能与水反应生成了碳酸,所以,溶液的pH小于7,反应的方程式是:H2O+CO2=H2CO3.
故答为:(1)铁架台,长颈漏斗;(2)2KClO3
2KCl+3O2↑,导管口有气泡连续均匀冒出时,2NaOH+SO2=Na2SO3+H2O; (3)BE,可以随时控制反应发生或停止,CaCO3+2HCl=CaCl2+H2O+CO2↑,b,efcd;(4)<;H2O+CO2=H2CO3.
(2)由A装置可知,此装置是加热固体制取气体的装置,如制取氧气,可用加热氯酸钾和二氧化锰混合物的方法,反应的方程式是:2KClO3
| ||
| △ |
(3)实验室用大理石和稀盐酸反应制取二氧化碳,反应物的状是固体和液体,反应条件是常温,应选用发生装置B,由于二氧化碳的密度大于空气的密度,可选用收集装置E;使用该套装置制取气体的突出优点是:可以随时控制反应发生或停止,该反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;若改用F装置收集二氧化碳,由于二氧化碳的密度大于空气的密度,则气体应从b 端进入.制得的二氧化碳中常含有少量的氯化氢气体与水蒸气,要将以上杂质气体除去,应先将氯化氢气体除去,在除去水蒸气.则装置正确的连接顺序是:混合气体→efcd;
(4)二氧化碳能与水反应生成了碳酸,所以,溶液的pH小于7,反应的方程式是:H2O+CO2=H2CO3.
故答为:(1)铁架台,长颈漏斗;(2)2KClO3
| ||
| △ |
点评:本题主要是对实验装置的选择,反应物的状态决定了制取装置,气体的溶解性和密度决定了收集方法,选择哪种装置主要看是否能控制反应的进行,节约药品等方面考虑.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案
相关题目
 (2012?定西)2011年7月3日,以“激情马拉松,活力新兰州”为口号的兰州国际马拉松赛成功落下帷幕.如图是用锌合金制作的此次活动的纪念章.锌合金属于( )
(2012?定西)2011年7月3日,以“激情马拉松,活力新兰州”为口号的兰州国际马拉松赛成功落下帷幕.如图是用锌合金制作的此次活动的纪念章.锌合金属于( )