题目内容
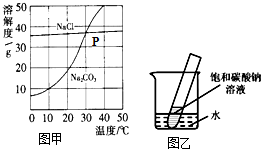 图甲为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线.请回答下列问题:
图甲为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线.请回答下列问题:(1)10℃时,碳酸钠的溶解度为
(2)P点表示
(3)当温度
(4)生活在盐湖附近的人们习惯“夏天晒盐,冬天捞碱”.请你解释原因:“冬天捞碱”
(5)如图乙所示,20℃时,将盛有饱和碳酸钠溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出.加入的物质可能是
A.氢氧化钠 B.生石灰 C.硝酸铵 D.浓硫酸.
分析:(1)运用碳酸钠的溶解度曲线解答.
(2)根据溶解度曲线相交的意义回答;
(3)根据溶解度曲线在上边的溶解度就大考虑;
(4)运用氯化钠的溶解度受温度影响小,碳酸钠的溶解度随温度的升高而而增大,对于溶解度受温度影响较大的物质,可以采用冷却热饱和溶液的方法得到晶体解答;
(5)运用物质溶于水后放热还是吸热和碳酸钠的溶解度随温度的升高而增大解答.
(2)根据溶解度曲线相交的意义回答;
(3)根据溶解度曲线在上边的溶解度就大考虑;
(4)运用氯化钠的溶解度受温度影响小,碳酸钠的溶解度随温度的升高而而增大,对于溶解度受温度影响较大的物质,可以采用冷却热饱和溶液的方法得到晶体解答;
(5)运用物质溶于水后放热还是吸热和碳酸钠的溶解度随温度的升高而增大解答.
解答:解:(1)10℃时,碳酸钠的溶解度为10g,故答案:10g.
(2)溶解度曲线中交点表示该温度下,两物质的溶解度相同;两条曲线的交点P表示的含义是在30℃时氯化钠和碳酸钠的溶解度相等;
(3)小于30℃时,碳酸钠的溶解度曲线在氯化钠溶解度曲线的下边,所以小于30℃时,碳酸钠的溶解度<氯化钠的溶解度;
(4)氯化钠的溶解度受温度影响小,碳酸钠的溶解度随温度的升高而增大对于溶解度受温度影响较大的物质,可以采用冷却热饱和溶液的方法得到晶体,故答案:冬天气温低,碳酸钠的溶解度随温度降低而降低.
(5)氢氧化钠、浓硫酸溶于水会放热,生石灰和水反应生成氢氧化钙会放出大量的热,碳酸钠的溶解度随温度的升高而增大;硝酸铵的溶解吸热温度降低,碳酸钠的饱和溶液会析出晶体,故答案:C.
故答案为:(1)10;(2)30℃时,碳酸钠与氯化钠的溶解度相同;(3)小于30℃;(4)碳酸钠的溶解度受温度影响大,冬天温度低,碳酸钠易结晶析出;(5)C.
(2)溶解度曲线中交点表示该温度下,两物质的溶解度相同;两条曲线的交点P表示的含义是在30℃时氯化钠和碳酸钠的溶解度相等;
(3)小于30℃时,碳酸钠的溶解度曲线在氯化钠溶解度曲线的下边,所以小于30℃时,碳酸钠的溶解度<氯化钠的溶解度;
(4)氯化钠的溶解度受温度影响小,碳酸钠的溶解度随温度的升高而增大对于溶解度受温度影响较大的物质,可以采用冷却热饱和溶液的方法得到晶体,故答案:冬天气温低,碳酸钠的溶解度随温度降低而降低.
(5)氢氧化钠、浓硫酸溶于水会放热,生石灰和水反应生成氢氧化钙会放出大量的热,碳酸钠的溶解度随温度的升高而增大;硝酸铵的溶解吸热温度降低,碳酸钠的饱和溶液会析出晶体,故答案:C.
故答案为:(1)10;(2)30℃时,碳酸钠与氯化钠的溶解度相同;(3)小于30℃;(4)碳酸钠的溶解度受温度影响大,冬天温度低,碳酸钠易结晶析出;(5)C.
点评:本题考查了从溶解度曲线图上读取信息、分析及获取信息的能力.从溶解度曲线可以看出:同一溶质在不同温度下的溶解度;同一温度下,不同溶质的溶解度;温度对不同物质的溶解度影响不同.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目

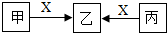 (2013?莆田)甲、乙、丙、X是初中化学常见的四中物质.它们的转化关系如图所示(部分产物略去,图中“
(2013?莆田)甲、乙、丙、X是初中化学常见的四中物质.它们的转化关系如图所示(部分产物略去,图中“