题目内容
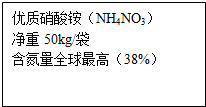 小强同学在公共场所围墙上看到一则化肥广告如图所示.回校后,小强通过计算氮的质量分量发现该广告是虚假广告.
小强同学在公共场所围墙上看到一则化肥广告如图所示.回校后,小强通过计算氮的质量分量发现该广告是虚假广告.(1)请你写出小强的计算过程和判断依据.
(2)这种化肥每袋量多含氮元素多少kg?
分析:(1)根据化合物中元素的质量分数=
×100%,进行分析解答.
(2)根据混合物元素的质量=该混合物质量×该元素的质量分数,进行分析解答.
| 相对原子质量×原子个数 |
| 相对分子质量 |
(2)根据混合物元素的质量=该混合物质量×该元素的质量分数,进行分析解答.
解答:解:(1)硝酸铵中氮元素的质量分数为:
×100%=35%,因为35%<38%,故该广告是虚假广告.
(2)假如是纯的硝酸铵,则每袋化肥中含氮元素的质量为50kg×35%=17.5kg.所以最多是含有17.5kg氮元素.
故答案为:(1)35%<38%,是虚假广告;(2)17.5kg.
| 14×2 |
| 14×2+1×4+16×3 |
(2)假如是纯的硝酸铵,则每袋化肥中含氮元素的质量为50kg×35%=17.5kg.所以最多是含有17.5kg氮元素.
故答案为:(1)35%<38%,是虚假广告;(2)17.5kg.
点评:本题难度不大,考查同学们结合标签新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
Ⅰ.成年人每分钟大约需要吸入8L氧气.问成年人每分钟大致需要空气 升;在标准状况下,8L氧气的质量是 克;所需空气的质量为 克;(空气中氧气体积分数按20%计算,氧气的密度=1.429g?L-1,空气的密度=1.293g?L-1).
Ⅱ.小强同学在公共场所围墙上看到一则化肥广告(如图).回校后,小强想通过计算氮的质量分数判断该广告是否
为虚假广告.
Ⅱ.小强同学在公共场所围墙上看到一则化肥广告(如图).回校后,小强想通过计算氮的质量分数判断该广告是否
为虚假广告.
| 国内首创 优质硝酸铵 NH4 NO3 含氮量全球最高(38%)(1)请你写出小强的计算过程和判断依据.计算过程: 结论:该广告 (2)小强认为此广告会坑害农民,向有关部门反映,技术监督局对该产品取样分析,发现氮元素质量分数仅为28%,则该产品中硝酸铵的质量分数为 |
 小强同学在公共场所围墙上看到一则化肥广告.
小强同学在公共场所围墙上看到一则化肥广告. (1)化肥尿素[CO(NH2)2]中碳、氧、氮、氢四种元素的原子个数比为
(1)化肥尿素[CO(NH2)2]中碳、氧、氮、氢四种元素的原子个数比为 小强同学在公共场所围墙上看到一则化肥广告(如图).回校后,小强通过计算氮的质量分数发现该广告是虚假广告.
小强同学在公共场所围墙上看到一则化肥广告(如图).回校后,小强通过计算氮的质量分数发现该广告是虚假广告. 小强同学在公共场所的围墙上看到一则化肥广告如下图:回校后,他做如下计算:
小强同学在公共场所的围墙上看到一则化肥广告如下图:回校后,他做如下计算: