题目内容
(9分)同学们对Na2CO3溶液也能使酚酞试液变红产生了兴趣。请你一同参与以下的实验探究。
【提出问题】碱溶液使酚酞试液变红,是因为碱在水中解离出OH﹣。Na2CO3属于 (选填“酸”、“碱”、“盐”);那么Na2CO3溶液中究竟是哪种粒子使酚酞试液变红呢?
【进行实验】同学们取了三份酚酞试液进行下图实验
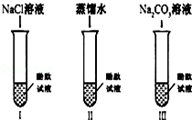
(1)实验I的目的是为了 ;
(2)实验Ⅱ加入蒸馏水的目的是探究水分子是否能使酚酞试液变红,小明同学认为实验Ⅱ没必要做,你认为小明的理由是 ;
(3)实验Ⅲ滴入Na2CO3溶液,振荡,酚酞试液变红,向变红后的溶液中再滴加过量的CaCl2溶液,振荡,红色逐渐消失,同时观察到生成 。
【得出结论】溶液中的CO32﹣使酚酞试液变红;
【交流反思】(4)老师看了同学们的探究结论说:“Na2CO3溶液使酚酞变红也是由于溶液中存在OH﹣。”你认为Na2CO3溶液中存在OH﹣的原因可能是 。
【拓展应用】同学们称取10g纯碱(杂质只有氯化钠)固体,将其加入50g稀盐酸中,恰好完全反应,使气体全部放出(忽略CO2在水中的溶解),得到氯化钠溶液56.7g。请计算:①反应中产生的CO2的质量;②纯碱中Na2CO3的质量分数。(请写出解题过程)
【提出问题】碱溶液使酚酞试液变红,是因为碱在水中解离出OH﹣。Na2CO3属于 (选填“酸”、“碱”、“盐”);那么Na2CO3溶液中究竟是哪种粒子使酚酞试液变红呢?
【进行实验】同学们取了三份酚酞试液进行下图实验

(1)实验I的目的是为了 ;
(2)实验Ⅱ加入蒸馏水的目的是探究水分子是否能使酚酞试液变红,小明同学认为实验Ⅱ没必要做,你认为小明的理由是 ;
(3)实验Ⅲ滴入Na2CO3溶液,振荡,酚酞试液变红,向变红后的溶液中再滴加过量的CaCl2溶液,振荡,红色逐渐消失,同时观察到生成 。
【得出结论】溶液中的CO32﹣使酚酞试液变红;
【交流反思】(4)老师看了同学们的探究结论说:“Na2CO3溶液使酚酞变红也是由于溶液中存在OH﹣。”你认为Na2CO3溶液中存在OH﹣的原因可能是 。
【拓展应用】同学们称取10g纯碱(杂质只有氯化钠)固体,将其加入50g稀盐酸中,恰好完全反应,使气体全部放出(忽略CO2在水中的溶解),得到氯化钠溶液56.7g。请计算:①反应中产生的CO2的质量;②纯碱中Na2CO3的质量分数。(请写出解题过程)
【提出问题】 盐
【进行实验】(1)探究Na+能否使酚酞试液变红 (2)NaCl溶液中有水分子
(3)白色沉淀(浑浊)
【交流反思】(4) CO32—(Na2CO3或碳酸钠)与H2O(水)反应产生OH—
【拓展应用】①3.3g ② 79.5%
【进行实验】(1)探究Na+能否使酚酞试液变红 (2)NaCl溶液中有水分子
(3)白色沉淀(浑浊)
【交流反思】(4) CO32—(Na2CO3或碳酸钠)与H2O(水)反应产生OH—
【拓展应用】①3.3g ② 79.5%
试题分析:【提出问题】Na2CO3由金属离子和酸根离子构成,属于盐
【进行实验】Na2CO3溶液中含有三种微粒:H2O、Na+、CO32-,要探究究竟是哪种粒子使酚酞试液变红,根据右图实验,采取的是逐一排除法,(1)实验I的目的是为了探究Na+能否使酚酞试液变红
(2)实验Ⅱ加入蒸馏水的目的是探究水分子是否能使酚酞试液变红,小明同学认为实验Ⅱ没必要做,你认为小明的理由是NaCl溶液中有水分子或酚酞溶液中本身含有水分子,但不变色
(3)实验Ⅲ滴入Na2CO3溶液,振荡,酚酞试液变红,向变红后的溶液中再滴加过量的CaCl2溶液,振荡,发生反应:CaCl2+Na2CO3==CaCO3↓+2NaCl,看到红色逐渐消失,同时观察到生成白色沉淀(浑浊)
【交流反思】(4)老师看了同学们的探究结论说:“Na2CO3溶液使酚酞变红也是由于溶液中存在OH﹣”Na2CO3溶液中存在OH﹣的原因可能是:CO32—(Na2CO3或碳酸钠)与H2O(水)反应产生OH—
【拓展应用】根据质量守恒定律:化学反应前后,物质的总质量不变,故①反应中产生的CO2的质量=10g+50g-56.7g=3.3g;在根据化学反应:Na2CO3+2HCl==2NaCl+H2O+CO2↑中Na2CO3与CO2的质量关系,即可求出Na2CO3的质量,进而可求解纯碱中Na2CO3的质量分数
解:②设纯碱中Na2CO3的质量为x
Na2CO3+2HCl
 2NaCl+CO2↑+H2O
2NaCl+CO2↑+H2O 106 44
x 3.3g
106:44=x:3.3g x=7.95g
Na2CO3% ="7.95g/10g×100%" = 79.5%
答:碳酸钠的质量分数为79.5%

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目



