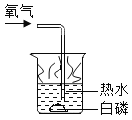
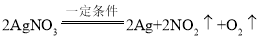题目内容
【题目】如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。据图回答:
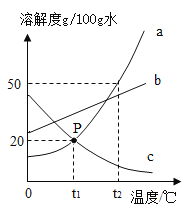
(1)P点的含义是_______________。
(2)t2℃时30ga物质加入到50g水中不断搅拌,形成__________g溶液。
(3)a物质中含有少量b,提纯固体a的方法是___________________。
(4)下列说法正确的是_______。
a.将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数大小关系是b>a>c
b.t2℃时a溶液的溶质质量分数可以为40%
c.t2℃时b的饱和溶液温度降低,溶质的质量分数减小
d.等质量的a和b的溶液分别由t2℃降到t1℃,a析出晶体的质量一定比b的多
【答案】t1℃时,a,c的溶解度等于20g 75 冷却热饱和溶液 ac
【解析】
(1) a与c的溶解度曲线相交于P点,故P点的含义是在t1℃时,a、c的溶解度相等,为20g。
(2)t2℃时,a物质的溶解度为50g,50g水能溶解的,a物质的质量为![]() ,故30ga物质加入到50g水中不断搅拌,能溶解25g,形成50g+25g=75g溶液。
,故30ga物质加入到50g水中不断搅拌,能溶解25g,形成50g+25g=75g溶液。
(3) a物质的溶解度随温度升高而增大,故从a的溶液中得到a固体的方法是冷却热饱和溶液。
(4) A、将t1℃时,a、c的溶解度相同,b的溶解度最大,温度升高到t2℃时,a、b溶液的溶质质量不变,c物质的溶解度随温度升高而减小,c有晶体析出,溶质质量减少,故a、b、c三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数大小关系是b>a>c,故a正确;
B、t2℃时,a物质的饱和溶液的质量分数为![]() ,则a溶液的溶质质量分数不能为40%,故b不正确;
,则a溶液的溶质质量分数不能为40%,故b不正确;
C、b物质的溶解度随温度升高而增大,t2℃时,b的饱和溶液温度降低,有晶体析出,溶液质量不变,则溶质的质量分数减小,故c正确;
D、a、b两种物质的溶解度随温度升高而增大,a物质的溶解度受温度的影响较大,等质量的a和b的饱和溶液分别由t2℃降到t1℃,a析出晶体的质量比b的多,题中没有确定溶液是否饱和,故d不正确。
故选ac。

 华东师大版一课一练系列答案
华东师大版一课一练系列答案【题目】梧州市某中学化学兴趣小组的同学到超市购买锡纸用于烧烤,同学们看见商品标签上标明锡纸的材质为“铝箔”。
(提出问题)锡纸的材质到底是锡还是铝呢?小吴认为可以把锡纸放入盐酸中观察是否有气体放出来区别是锡还是铝,小周同学认为这样不能区别,理由是___________。
小施查阅资料发现锡的熔点是232 ℃,而铝的熔点为660 ℃,他用_______的方法区别出锡纸的材质是铝不是锡,接着同学们对铝这种金属进行了探究。
(探究活动一)铝的含量分析
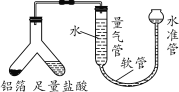
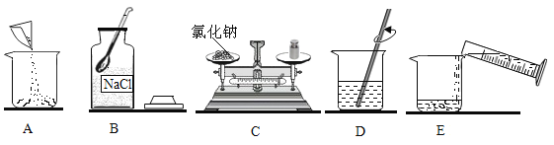
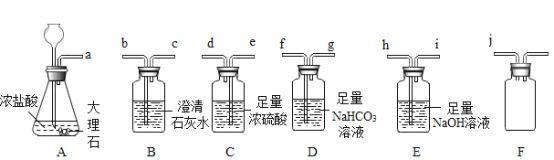
(1)小施用如图装置测定铝箔中金属铝的含量,检验该装置气密性的操作是___________。
(2)若测得进入量气管的气体体积为100 mL(氢气的密度为0.09 g/L),铝箔中金属铝的质量为______ g(铝箔中只有铝能与盐酸反应生成气体)。
(探究活动二)铝箔燃烧
同学们做铝箔燃烧的实验。小吴用坩埚钳夹持一小块铝箔放在酒精灯火焰上,轻轻晃动,观察到铝箔熔化,失去了光泽,但铝箔并不燃烧;小周另取一块铝箔,用砂纸仔细打磨,再用坩埚钳夹持放在酒精灯火焰上,观察到铝箔仍不能燃烧。
(1)小施同学认为铝箔不能在空气中燃烧是因为__________。
(2)小施同学改进了实验,让铝箔燃烧并发出了耀眼的白光,小施同学的实验方案是_________。
(探究活动三)小吴将打磨后的铝片与铜盐溶液反应,现象如下:
实验一:4 mL 8%的CuSO4溶液 | 实验二:4 mL 8%的CuCl2溶液 | |
实验 现象 | 短时间内无变化,一段时间后铝片上才出现少量红色的铜 | 铝片上迅速有红色的铜出现 |
(1)铝与氯化铜溶液反应的化学方程式为__________。
(2)对比两个实验,小周推测对铝与铜盐溶液的反应可能有促进作用的离子是__________(填写离子符号),为了验证此推测,小施向实验一的CuSO4溶液中加入1g________(填写化学式)固体,立即观察到铝片上出现大量红色的铜。