题目内容
有炭粉和氧化铜的黑色固体20g,加热后将生成的气体通入足量的石灰水中,气体全被吸收,产生了10g沉淀,求原混合物的组成。
【答案】
C:1.2g,CuO:18.8g或CuO:16g ,C:4g
【解析】
试题分析:炭粉和氧化铜的黑色固体20g,加热反应要不恰好反应,要不炭粉过量,要不氧化铜过量,发生反应;C+ 2CuO? 高温 2Cu + CO2↑,生成的气体通入足量的石灰水中,方程式:Ca(OH)2 +CO2 =CaCO3↓+H2O,,沉淀质量10g即CaCO3的质量,再根据化学方程式可得以下关系式:CaCO3 ≈? CO2 ≈? C? ≈? 2CuO,,即可算出
解:设参加反应C的质量为x,CuO质量为y
Ca(OH)2 +CO2 =CaCO3↓+H2O??? C + 2CuO 2Cu + CO2↑
2Cu + CO2↑
根据化学方程式可得以下关系式:
CaCO3 ≈? CO2 ≈? C? ≈? 2CuO
100?????? 44????? 12????? 160
10g??????????????? x?????? y
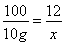
x=1.2g
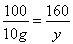
y=16g
原混合物的组成:C:1.2g,CuO:18.8g或CuO:16g ,C:4g
考点:化学方程式中物质的过量的计算

练习册系列答案
相关题目