题目内容
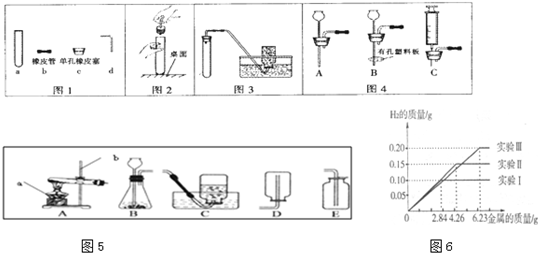
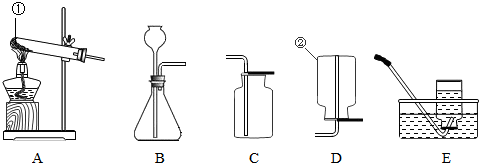
化学是一门以实验为基础的科学,化学所取得的丰硕成果,是与实验的重要作用分不开的.结合下列实验装置图(如图1)回答问题:
(1)写出指定仪器的名称:①______ ②______
(2)下面四种途径都可以得到氧气(如图2):

写出实验室中通过甲、乙两种途径制取氧气的文字表达式甲______
【答案】分析:(1)熟悉掌握实验装置中的仪器名称并会书写;
(2)根据题意分别写出制取氧气的甲、乙两个化学方程式;
(3)依据题意从实现原料和反应过程中的反应装置、反应条件的绿色化考虑甲、乙、丙三途径谁更能体现化学实验的绿色化追求.
(4)由高锰酸钾制取氧气时选择固态物质反应加热装置,注意用排水法收集完氧气后的先后操作顺序,避免操作失误造成不良后果.
(5)根据信息:实验室常用氯化铵固体与碱石灰固体共热来制取氨气.常温下NH3是一种无色、有刺激性气味的气体,密度比空气小.NH3极易溶于水.分析解答.
(6)根据一氧化氮难溶于水,密度比空气略大,在空气中能与氧气迅速反应生成红棕色的二氧化氮气体分析.
(7)氧气钢瓶中的氧气是干燥的,如果直接进入人体会使人感觉到不舒服,而且无法控制氧气的流速,此装置中水的作用一是湿润氧气,二是控制氧气的流速,所以气体应从a端进入.
解答:解:(1)图中①是试管,②是集气瓶.
故答案为:试管;集气瓶.
(2)根据题意分别写出制取氧气的甲、乙两种途径制取氧气的文字表达式甲:过氧化氢 水+氧气;乙:高锰酸钾
水+氧气;乙:高锰酸钾 锰酸钾+二氧化锰+氧气.
锰酸钾+二氧化锰+氧气.
故答案为:过氧化氢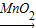 水+氧气;高锰酸钾
水+氧气;高锰酸钾 锰酸钾+二氧化锰+氧气.
锰酸钾+二氧化锰+氧气.
(3)从实现原料和反应过程的绿色化考虑,甲途径采用过氧化氢溶液加二氧化锰在常温下反应,乙途径采用高锰酸钾在加热时反应,丙途径采用氯酸钾和二氧化锰在加热时反应,在乙、丙途径中都需加热,在操作实验中既麻烦又浪费能源,故甲途径更体现化学实验的绿色化追求.
故答案为:甲.
(4)用高锰酸钾制取氧气时选择固态物质反应加热装置,故选用A装置.用排水收集氧气完毕后,停止加热时的操作顺序是先把导管移出水面,然后熄灭酒精灯;如先熄灭酒精灯,大试管内温度降低,气压减小,致使水倒吸进入热的试管中,造成试管破裂.
故答案为:A;撤出试管;熄灭酒精灯.
(5)实验室常用氯化铵固体与碱石灰固体共热来制取氨气,是固体的加热反应,所以用装置A作发生装置;密度比空气小.NH3极易溶于水,所以用向下排空气法收集.
选择气体收集方法与气体的密度和溶水性有关,不易溶于水的可以用排水法收集,密度大于空气密度的用向上排空气法,密度小于空气密度的用向下排空气法.
故答案为:A;D;气体的密度;溶水性.
(6)一氧化氮难溶于水,密度比空气略大,在空气中能与氧气迅速反应生成红棕色的二氧化氮气体,所以不能用排空气法收集,可用排水法收集.
故答案为:E.
(7)此装置中的蒸馏水的作用是为了湿润氧气钢瓶中进入的氧气,同时因为氧气不易溶于水,所以从气泡的流速来控制氧气的输入量,由以上用途可知,装置a端应接氧气钢瓶,b端应接病人吸氧器.
故答案为:a;观察氧气的流速(或湿润氧气,答案合理即可.)
点评:此题主要考查根据反应物状态和反应条件选择实验室制取气体的实验装置,根据收集气体的性质选择收集方法及注意事项,此题设计开放,锻炼学生的良好思维能力.
(2)根据题意分别写出制取氧气的甲、乙两个化学方程式;
(3)依据题意从实现原料和反应过程中的反应装置、反应条件的绿色化考虑甲、乙、丙三途径谁更能体现化学实验的绿色化追求.
(4)由高锰酸钾制取氧气时选择固态物质反应加热装置,注意用排水法收集完氧气后的先后操作顺序,避免操作失误造成不良后果.
(5)根据信息:实验室常用氯化铵固体与碱石灰固体共热来制取氨气.常温下NH3是一种无色、有刺激性气味的气体,密度比空气小.NH3极易溶于水.分析解答.
(6)根据一氧化氮难溶于水,密度比空气略大,在空气中能与氧气迅速反应生成红棕色的二氧化氮气体分析.
(7)氧气钢瓶中的氧气是干燥的,如果直接进入人体会使人感觉到不舒服,而且无法控制氧气的流速,此装置中水的作用一是湿润氧气,二是控制氧气的流速,所以气体应从a端进入.
解答:解:(1)图中①是试管,②是集气瓶.
故答案为:试管;集气瓶.
(2)根据题意分别写出制取氧气的甲、乙两种途径制取氧气的文字表达式甲:过氧化氢
 水+氧气;乙:高锰酸钾
水+氧气;乙:高锰酸钾 锰酸钾+二氧化锰+氧气.
锰酸钾+二氧化锰+氧气.故答案为:过氧化氢
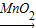 水+氧气;高锰酸钾
水+氧气;高锰酸钾 锰酸钾+二氧化锰+氧气.
锰酸钾+二氧化锰+氧气.(3)从实现原料和反应过程的绿色化考虑,甲途径采用过氧化氢溶液加二氧化锰在常温下反应,乙途径采用高锰酸钾在加热时反应,丙途径采用氯酸钾和二氧化锰在加热时反应,在乙、丙途径中都需加热,在操作实验中既麻烦又浪费能源,故甲途径更体现化学实验的绿色化追求.
故答案为:甲.
(4)用高锰酸钾制取氧气时选择固态物质反应加热装置,故选用A装置.用排水收集氧气完毕后,停止加热时的操作顺序是先把导管移出水面,然后熄灭酒精灯;如先熄灭酒精灯,大试管内温度降低,气压减小,致使水倒吸进入热的试管中,造成试管破裂.
故答案为:A;撤出试管;熄灭酒精灯.
(5)实验室常用氯化铵固体与碱石灰固体共热来制取氨气,是固体的加热反应,所以用装置A作发生装置;密度比空气小.NH3极易溶于水,所以用向下排空气法收集.
选择气体收集方法与气体的密度和溶水性有关,不易溶于水的可以用排水法收集,密度大于空气密度的用向上排空气法,密度小于空气密度的用向下排空气法.
故答案为:A;D;气体的密度;溶水性.
(6)一氧化氮难溶于水,密度比空气略大,在空气中能与氧气迅速反应生成红棕色的二氧化氮气体,所以不能用排空气法收集,可用排水法收集.
故答案为:E.
(7)此装置中的蒸馏水的作用是为了湿润氧气钢瓶中进入的氧气,同时因为氧气不易溶于水,所以从气泡的流速来控制氧气的输入量,由以上用途可知,装置a端应接氧气钢瓶,b端应接病人吸氧器.
故答案为:a;观察氧气的流速(或湿润氧气,答案合理即可.)
点评:此题主要考查根据反应物状态和反应条件选择实验室制取气体的实验装置,根据收集气体的性质选择收集方法及注意事项,此题设计开放,锻炼学生的良好思维能力.

练习册系列答案
相关题目
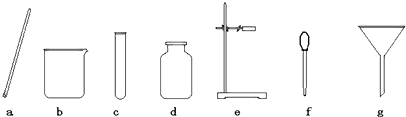
 20、化学是一门以实验为基础的科学,规范的实验操作是实验成功的前提,请回答:
20、化学是一门以实验为基础的科学,规范的实验操作是实验成功的前提,请回答: