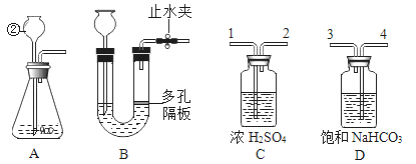
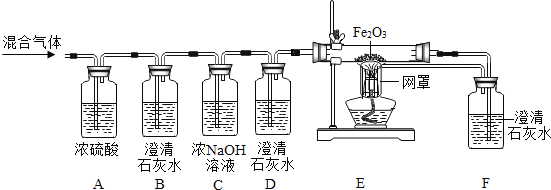
题目内容
【题目】某钙片的标签如图所示,可知此钙片成分中只有碳酸钙含有钙元素。

⑴请通过计算说明此标签中的含钙量是否错误。
⑵为测定其真实的含钙量,辉明同学每次取10片钙片放入已称量的含足量盐酸的烧杯中,充分反应后再称取烧杯和剩余物的总质量。辉明同学做了三次实验,数据如下:
物质的质量 | 第一次 | 第二次 | 第三次 | 平均值 |
反应前:烧杯+盐酸 | 22g | 22g | 22g | 22g |
10片钙片 | 8g | 8g | 8g | 8g |
反应后:烧杯+剩余物 | 26.7g | 26.5g | 26.9g | 26.7g |
【答案】标签中的含钙量是错误的;每片此钙片含钙的质量为0.3g。
【解析】
(1)先计算出碳酸钙中钙元素的质量分数,再计算出每片钙片中含有钙元素的质量,与标签中的含钙量相比较,判断此标签中的含钙量是否错误;(2)根据三次实验的平均值和质量守恒定律,反应前烧杯和反应物的质量总和-反应后烧杯和剩余物的质量即是生成二氧化碳气体的质量;然后根据碳酸钙与盐酸反应的化学方程式计算出参加反应的碳酸钙的质量(即10片钙片的质量),进而计算出每片此钙片含碳酸钙的质量。
解:(1)本品若为纯碳酸钙,碳酸钙的相对分子质量为100,钙元素的质量分数为![]() ×100%=40%,每片含钙量为:
×100%=40%,每片含钙量为:![]() ×40%=0.32g,因此本品每片不可能含钙0.75g,此标签中的含钙量错误;
×40%=0.32g,因此本品每片不可能含钙0.75g,此标签中的含钙量错误;
(2)生成二氧化碳气体的质量为:22g+8g-26.7g=3.3g,设10片钙片含碳酸钙的质量为x,
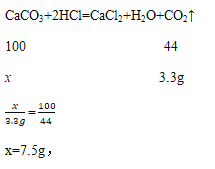
因此每片此钙片含碳酸钙的质量为7.5g÷10=0.75g,每片此钙片的含钙量为0.75g×40%=0.3g;
答:(1)标签中的含钙量是错误的;(2)每片此钙片含钙的质量为0.3g。

【题目】如图为自来水厂净水过程示意图.回答下列问题:
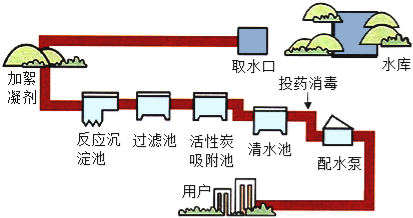
(1)在这个过程中,未涉及的净水方法是 (填序号)
A.吸附 | B.沉淀 | C.过滤 | D.煮沸 |
(2)水体污染日益严重,造成水体污染的来源主要有 、农业污染和生活污染.
(3)自然界中的水有硬水和软水,常用 来区分.
(4)天然水中常含有有害细菌,需消毒后才能饮用.近年来,用环保高效的新型消毒剂ClO2进行消毒.则ClO2中Cl的化合价是 .
(5)节约水资源已成为人类的共识.请列举一种可行的节水方法: .