题目内容
t℃时的KNO3溶液,恒温蒸发Ag水时,析出晶体ag;再恒温蒸发Ag水双析出晶体bg(a≠b),回答下列问题(1)ab(“>”或“<”)(2)t℃时KNO3的溶解度为g.
【答案】分析:t℃时的KNO3溶液的状态未明确,所以首先通过两次恒温蒸发相同质量的水Ag析出晶体的质量推断此溶液是否饱和.
根据t℃时的KNO3饱和溶液中溶质和溶剂的质量,利用公式:溶解度= 求出该温度下的溶解度.
求出该温度下的溶解度.
解答:解:(1)两次恒温蒸发相同质量的水而析出晶体质量却不相等,说明第一次进行蒸发时的溶液不是饱和溶液,蒸发时先蒸发掉部分水使溶液变为饱和溶液,此时未有晶体析出,然后继续蒸发才有晶体随之不断析出.所以,第一次蒸发所得晶体质量小于随后进行的第二次蒸发.
故答:<;
(2)第二次恒温蒸发时溶液为饱和溶液,所以析出的晶体bg就是蒸发Ag水达饱和时溶解溶质的量;即在t℃时Ag水溶解溶解bgKNO3达饱和,此时KNO3的溶解度=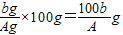 .
.
故答: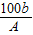
点评:恒温蒸发饱和溶液析出晶体的质量就是蒸发掉的水在该温度所能溶解溶质的最大量.
根据t℃时的KNO3饱和溶液中溶质和溶剂的质量,利用公式:溶解度=
 求出该温度下的溶解度.
求出该温度下的溶解度.解答:解:(1)两次恒温蒸发相同质量的水而析出晶体质量却不相等,说明第一次进行蒸发时的溶液不是饱和溶液,蒸发时先蒸发掉部分水使溶液变为饱和溶液,此时未有晶体析出,然后继续蒸发才有晶体随之不断析出.所以,第一次蒸发所得晶体质量小于随后进行的第二次蒸发.
故答:<;
(2)第二次恒温蒸发时溶液为饱和溶液,所以析出的晶体bg就是蒸发Ag水达饱和时溶解溶质的量;即在t℃时Ag水溶解溶解bgKNO3达饱和,此时KNO3的溶解度=
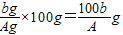 .
.故答:
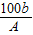
点评:恒温蒸发饱和溶液析出晶体的质量就是蒸发掉的水在该温度所能溶解溶质的最大量.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目