题目内容
分析HCl、X、HClO、KClO3、KClO4的排列顺序规律,可知X代表的是( )
| A、NaCl |
| B、Ca(ClO)2 |
| C、Cl2 |
| D、Cl2O |
考点:有关元素化合价的计算
专题:化学式的计算
分析:根据单质中元素的化合价为0、在化合物中正负化合价代数和为零,分别计算HCl、HClO、KClO3、KClO4中氯元素的化合价,找出化合价排列规律;确定所给选项的四种物质中氯元素化合价,找出符合这一规律的物质.
解答:解:在化合物中正负化合价代数和为零,HCl、HClO、KClO3、KClO4中氯元素的化合价分别为-1、+1、+5、+7,可得出:物质是按氯元素化合价由低到高进行排列,则X中氯元素化合价应在-1和+1之间.
A、钠元素显+1价,设氯元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x=0,则x=-1.
B、钙元素显+2价,氧元素显-2价,设氯元素的化合价是y,根据在化合物中正负化合价代数和为零,可得:(+2)+2y+(-2)×2=0,则y=+1.
C、单质中元素的化合价为0,因此氯气中氯元素化合价为0.
D、氧元素显-2价,设氯元素的化合价是z,根据在化合物中正负化合价代数和为零,可得:2z+(-2)=0,则z=+1.
C选项中氯元素化合价在-1和+1之间,符合要求.
故选:C.
A、钠元素显+1价,设氯元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x=0,则x=-1.
B、钙元素显+2价,氧元素显-2价,设氯元素的化合价是y,根据在化合物中正负化合价代数和为零,可得:(+2)+2y+(-2)×2=0,则y=+1.
C、单质中元素的化合价为0,因此氯气中氯元素化合价为0.
D、氧元素显-2价,设氯元素的化合价是z,根据在化合物中正负化合价代数和为零,可得:2z+(-2)=0,则z=+1.
C选项中氯元素化合价在-1和+1之间,符合要求.
故选:C.
点评:本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法即可正确解答.

练习册系列答案
相关题目
下列有关数据合理的是( )
| A、用托盘天平称取65.48克食盐 |
| B、用镊子取0.1克砝码 |
| C、用量筒量取44.15mL的硫酸铜溶液 |
| D、用托盘天平称取13.0克氯化钠 |
实验操作考查时,要求考生配制50g 5%的NaCl溶液,所给仪器都会用到的一组是( )
| A、胶头滴管 玻璃棒 烧杯 漏斗 |
| B、托盘天平 烧杯 量筒 玻璃棒 |
| C、量筒 烧杯 托盘天平 试管 |
| D、酒精灯 量筒 托盘天平 烧杯 |
下列操作不会造成药品污染的是( )
| A、实验剩余的药品放回原瓶 |
| B、倒液体时,将瓶塞正放在桌上 |
| C、将滴管用清水清洗后,再吸另一药品 |
| D、滴管滴液时,伸进试管里并碰在管壁上 |
下列说法错误的是( )
| A、分子是保持物质化学性质的最小粒子 |
| B、任何物质都是由分子构成的 |
| C、由同一种元素组成的物质不一定是单质 |
| D、元素是具有相同核电荷数的一类原子的总称 |
 如图表示了初中化学中一些常见物质的相互转化关系(部分反应条件已省略).下列说法错误的是( )
如图表示了初中化学中一些常见物质的相互转化关系(部分反应条件已省略).下列说法错误的是( )| A、圈Ⅰ中发生的反应可能都是分解反应 |
| B、利用反应②可用来检验二氧化碳气体 |
| C、圈Ⅱ中的化学反应说明氧气具有可燃性 |
| D、利用反应①可制得烧碱 |
下列性质属于氧气化学性质的是( )
| A、氧气可以燃烧 |
| B、氧气密度比空气略大 |
| C、氧气不易溶于水 |
| D、氧气具有氧化性 |
雯雯同学所做的下列实验中,不发生化学变化的是( )
A、 探究铁钉生锈 |
B、 探究分子运动 |
C、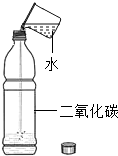 探究二氧化碳性质 |
D、 探究燃烧条件 |