题目内容
【题目】学习化学离不开实验
(1)在实验课上,老师要同学们配制15%的氯化钠溶液50 g。
①计算:配制15%的氯化钠溶液50 g,需氯化钠的质量为_____________g。
②甲同学按下图所示步骤依次操作。
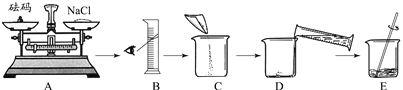
其错误的操作步骤有_______(填字母序号);E中玻璃棒的作用是_________________。
③乙同学在将称量好的氯化钠倒入烧杯时,有一部分氯化钠固体撒出,则所配溶液溶质质量分数与15%相比___________(填“偏低”、“偏高”、或“相等”)
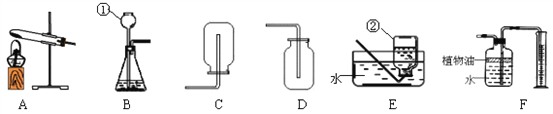
(2)请根据下图装置,回答相关问题:
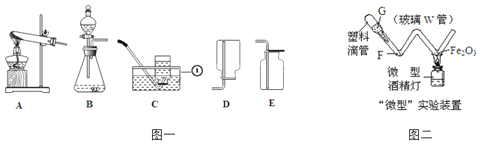
①写出图一中标号①的仪器名称:____________。
②实验室用过氧化氢溶液制取O2,可选用的发生装置为______(填写图一中装置序号)。
③小红想利用A装置通过加热高锰酸钾制氧气,此发生装置中还缺少的一种实验用品是______________。加热高锰酸钾制氧气的反应方程式为:_____________________。
④图二为某种“微型”实验装置。如果G处装稀盐酸,F处放少量锌粒,进行氢气还原氧化铁的实验;写出用“微型”装置进行该实验具有的一个优点:_____________。
【答案】 7.5 AB 搅拌,加快溶解 偏低 水槽 B 棉花 2KMnO4![]() K2MnO4 + MnO2 + O2↑ 节约药品用量或减少污染(合理即可)
K2MnO4 + MnO2 + O2↑ 节约药品用量或减少污染(合理即可)
【解析】(1)①50g 15%的氯化钠溶液中氯化钠的质量=50g×15%=7.5g;②错误的操作步骤有 A,没有按照左物右码的规定称量药品,B没有平视凹液面的最低处;E中玻璃棒的作用是搅拌,加速溶解;③配制溶液过程中,溶质损失,溶液的溶质质量分数会减小;(2)
根据实验室常用仪器可知:①是水槽;②实验室用过氧化氢溶液制取O2,属于固液常温型,故选B;③加热高锰酸钾制氧气,为防止高锰酸钾随气流进入导气管,试管口应放一团棉花;加热高锰酸钾制氧气的反应方程式为: ![]()
![]()
![]() ;④锌和硫酸反应生成氢气,氢气具有还原性,还原氧化铁时,红色会变成黑色;实验装置改进的优点是:节约药品、比较环保、安全等。
;④锌和硫酸反应生成氢气,氢气具有还原性,还原氧化铁时,红色会变成黑色;实验装置改进的优点是:节约药品、比较环保、安全等。

【题目】三明市民新水泥厂化验室,为了测定其矿山石灰石中碳酸钙的质量分数,取石灰石样品与是量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水)。有关实验数据如下表:
反应前 | 反应后 | ||
实验数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
150g | 12g | 157.6g | |
(1)根据质量守恒定律可知,反应中生成二氧化碳的质量为_______g。
(2)求该石灰石中碳酸钙的质量分数为__________。