题目内容
已知,在标准状况下,32克O2的体积是22.4升,O2在空气中的体积分数为21%,每克葡萄糖[C6H12O6]分解时产生的热量为17.15千焦.解答下列问题:(1)在静卧休息的情况下,某中等身材的男子一昼夜需要消耗约5858千焦的能量.若他由于某种疾病不能进食,只能靠输液维持,则一昼夜内至少需输入5%葡萄糖溶液( )
A.约13600ml B.约6800ml C.约3400ml D.约1700ml
(2)将某健康成人平静状态下的呼出气体作分析,结果O2的体积分数为16%,呼出气量为每分钟5.6升(已折算为标准状态下的值,不考虑水蒸气的影响).则该人每分钟消耗有机物(只考虑葡萄糖,完全氧化分解)多少克?该人当时的消耗功率多大?
分析:(1)由题中的信息“每克葡萄糖[C6H12O6]分解时产生的热量为17.15千焦”和“一昼夜内至少需输入5%葡萄糖溶液”进行计算;
(2)根据题目中的反应物、生成物和反应条件,依据化学方程式的书写方法,可以写出葡萄糖完全氧化分解的化学方程式;根据化学方程式找出葡萄糖与氧气的质量比,由氧气的质量可计算出葡萄糖的质量.
(2)根据题目中的反应物、生成物和反应条件,依据化学方程式的书写方法,可以写出葡萄糖完全氧化分解的化学方程式;根据化学方程式找出葡萄糖与氧气的质量比,由氧气的质量可计算出葡萄糖的质量.
解答:解:(1)设一昼夜内至少需输入5%葡萄糖溶液ymL,则:5858÷17.15=5%y,解得y≈6831
故选B
(2)每分钟消耗氧气的体积为5.6L×(21%-16%)=0.28L(因为氧气被消耗,才导致体积分数减小)
折算成质量为
×32g=0.4g
该人每分钟消耗的有机物的质量为x
C6H12O6+6O2
6CO2+6H2O
180 192
x 0.4g
=
x=0.375克
功率 P=
=
=107.2瓦
答:该人每分钟消耗有机物(只考虑葡萄糖,完全氧化分解)0.375克;该人当时的消耗功率是107.2瓦.
故选B
(2)每分钟消耗氧气的体积为5.6L×(21%-16%)=0.28L(因为氧气被消耗,才导致体积分数减小)
折算成质量为
| 0.28L |
| 22.4L |
该人每分钟消耗的有机物的质量为x
C6H12O6+6O2
| 酶 |
180 192
x 0.4g
| 180 |
| x |
| 192 |
| 0.4g |
x=0.375克
功率 P=
| W |
| t |
| 0.375×17150焦 |
| 60秒 |
答:该人每分钟消耗有机物(只考虑葡萄糖,完全氧化分解)0.375克;该人当时的消耗功率是107.2瓦.
点评:本题以葡萄糖,完全氧化分解反应为实验原理,将实验数据呈现,考查了阅读、分析、处理数据和化学计算的能力.

练习册系列答案
相关题目
如图所示,A、B为实验室制取某种气体的实验装置,
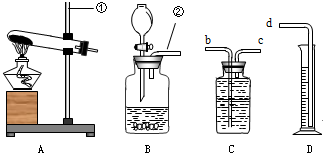
请回答下列问题:
(1)图中编号仪器的名称分别为:① ,② ;
(2)从反应物状态和反应条件来比较装置A和装置B的差异.
(3)利用装置A、C、D可粗略测定加热2g高锰酸钾所收集的氧气体积,A、C、D三装置的连接顺序是(填接口的字母):
A→ , →d.
(4)请根据化学方程式计算,2g 高锰酸钾完全分解理论上可生成标准状况下的氧气约多少升?(已知氧气在标准状况下的密度为1.429g/L).

请回答下列问题:
(1)图中编号仪器的名称分别为:①
(2)从反应物状态和反应条件来比较装置A和装置B的差异.
| 装置A | 装置B | |
| 反应物状态 | ||
| 反应条件 |
A→
(4)请根据化学方程式计算,2g 高锰酸钾完全分解理论上可生成标准状况下的氧气约多少升?(已知氧气在标准状况下的密度为1.429g/L).
钢铁的生产和使用是人类文明和社会进步的一个重要标志.
(1)每年钢铁锈蚀造成巨大的损失,铁制品锈蚀的主要原因是 .
(2)校课外兴趣小组取潍坊某钢铁厂生铁样品进行实验:将四份不同质量的生铁样品(假定其中只含单质铁和单质碳)分别加到100g质量分数相同的硫酸溶液中,充分反应后,测得的实验数据如下表所示:(已知:在标准状况下,22.4L H2的质量为2g)
通过计算回答下列问题:
①上述表格中m的值为 ;
②根据表中数据计算硫酸溶液中H2SO4的质量分数.
(1)每年钢铁锈蚀造成巨大的损失,铁制品锈蚀的主要原因是
(2)校课外兴趣小组取潍坊某钢铁厂生铁样品进行实验:将四份不同质量的生铁样品(假定其中只含单质铁和单质碳)分别加到100g质量分数相同的硫酸溶液中,充分反应后,测得的实验数据如下表所示:(已知:在标准状况下,22.4L H2的质量为2g)
| 实验序号 | 1 | 2 | 3 | 4 |
| 生铁样品的质量/g | 2.88 | 5.76 | 9.24 | 10.28 |
| 生成H2的体积(标准状况下)/L | 1.12 | 2.24 | 3.36 | m |
①上述表格中m的值为
②根据表中数据计算硫酸溶液中H2SO4的质量分数.