题目内容
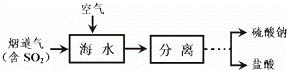
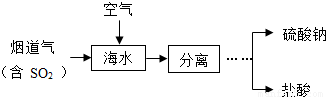
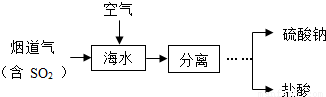
工业上利用海水法脱硫的工艺流程如图.请回答:(1)下列说法正确的是 (填字母).
A.此工艺要求设备耐腐蚀
B.使用此废气处理装置可以减少酸雨的形成
(2)此工艺流程的总化学反应方程式为: .
【答案】分析:(1)根据工艺流程中设计到酸,酸具有腐蚀性考虑,根据酸雨形成的主要原因考虑能否减少酸雨形成;(2)根据方程式的书写注意事项写出方程式.
解答:解:(1)二氧化硫与水结合生成亚硫酸,被空气中氧气氧化为硫酸,最后生成盐酸,硫酸和盐酸都具有腐蚀性,所以此工艺要求设备耐腐蚀;二氧化硫是形成酸雨的主要成分,该流程吸收了二氧化硫,所以使用此废气处理装置可以减少酸雨的形成;
(2)反应物是二氧化硫、氧气、水、氯化钠写在等号的左边,生成物是硫酸钠和盐酸写在等号的右边,用观察法配平即可,所以总方程式是:
2SO2+O2+2H2O+4NaCl═2Na2SO4+4HCl.
故答案为:(1)AB;(2)2SO2+O2+2H2O+4NaCl═2Na2SO4+4HCl.
点评:解答本题关键是要知道酸具有腐蚀性,二氧化硫是形成酸雨的主要气体,熟悉方程式的书写方法.
解答:解:(1)二氧化硫与水结合生成亚硫酸,被空气中氧气氧化为硫酸,最后生成盐酸,硫酸和盐酸都具有腐蚀性,所以此工艺要求设备耐腐蚀;二氧化硫是形成酸雨的主要成分,该流程吸收了二氧化硫,所以使用此废气处理装置可以减少酸雨的形成;
(2)反应物是二氧化硫、氧气、水、氯化钠写在等号的左边,生成物是硫酸钠和盐酸写在等号的右边,用观察法配平即可,所以总方程式是:
2SO2+O2+2H2O+4NaCl═2Na2SO4+4HCl.
故答案为:(1)AB;(2)2SO2+O2+2H2O+4NaCl═2Na2SO4+4HCl.
点评:解答本题关键是要知道酸具有腐蚀性,二氧化硫是形成酸雨的主要气体,熟悉方程式的书写方法.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
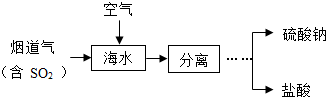 (2013?镇江模拟)工业上利用海水法脱硫的工艺流程如图.请回答:
(2013?镇江模拟)工业上利用海水法脱硫的工艺流程如图.请回答: