题目内容
【题目】为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水).有关数据如下表:
反应前 | 反应后 | ||
实验数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
150g | 12g | 157.6g |
(1)反应中生成二氧化碳的质量为多少?
(2)求该石灰石中碳酸钙的质量分数.
【答案】(1)4.4g (2)83.3%
【解析】
(1)根据质量守恒定律可以知道生成二氧化碳的质量为:150g+12g-157.6g=4.4g;
(2)设l2g该石灰石样品中碳酸钙的质量为x,则:
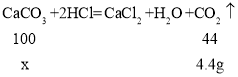
![]()
解得:x=10g
l2g该石灰石样品中碳酸钙的质量分数为:![]() ×100%≈83.3%
×100%≈83.3%
答:(1)反应中生成二氧化碳的质量是 4.4g;
(2)l2g该石灰石样品中碳酸钙的质量分数83.3%。

练习册系列答案
相关题目