题目内容
图表是二氧化锰用量与一定质量氯酸钾制取氧气反应速率关系的实验数据
(1)写出该反应的方程式:
(2)据上表可知二氧化锰与氯酸钾的质量比为 时,反应速率最快;
(3)二氧化锰的用量过少时产生氧气的速率很慢,原因是 ;
(4)二氧化锰用量过多冲淡了氯酸钾粉末,相当于减少反应物的 ,所以反应速率受到影响;
(5)通过分析可知,在化学反应中催化剂的用量(填“是”或“不是”) 越多越好.
| MnO2与KClO3质量比 | 1:40 | 1:20 | 1:10 | 1:5 | 1:3 | 1:2 | 2:3 | 1:1 | 2:1 |
| 生成1L氧气所需时间 | 124s | 79s | 50s | 54s | 75s | 93s | 106s | 153s | 240s |
(2)据上表可知二氧化锰与氯酸钾的质量比为
(3)二氧化锰的用量过少时产生氧气的速率很慢,原因是
(4)二氧化锰用量过多冲淡了氯酸钾粉末,相当于减少反应物的
(5)通过分析可知,在化学反应中催化剂的用量(填“是”或“不是”)
考点:催化剂的特点与催化作用,书写化学方程式、文字表达式、电离方程式
专题:空气与水
分析:(1)根据反应物和产物以及反应条件书写化学方程式;
(2)由表格内容发现其规律,知道所用时间与反应速度的关系考虑;
(3)根据反应速度的影响因素主要是反应物的接触面积来考虑;
(4)根据混合物的混合情况考虑,催化剂多了相对来说反应物就少了,反应速度就收到了影响;
(5)由实验现象分析结论,再通过表格上的数据能看出催化剂的用量与反应速度的关系.
(2)由表格内容发现其规律,知道所用时间与反应速度的关系考虑;
(3)根据反应速度的影响因素主要是反应物的接触面积来考虑;
(4)根据混合物的混合情况考虑,催化剂多了相对来说反应物就少了,反应速度就收到了影响;
(5)由实验现象分析结论,再通过表格上的数据能看出催化剂的用量与反应速度的关系.
解答:解:(1)该反应的化学方程式为:2KClO3
2KCl+3O2↑;
(2)通过表格可知所需要的时间越短,反应的速度就越快,所以二氧化锰与氯酸钾的质量比为1:10时,反应速度最快;
(3)反应速度的影响因素主要是反应物的接触面积,接触面积越大反应速度就越快,二氧化锰的用量过少与氯酸钾的接触面积就越小,所以反应速度慢;
(4)二氧化锰用量过多氯酸钾的质量分数就降低了,反应物的接触面积就少了,就影响了反应速度;
(5)通过上面的表格显示的内容可知在化学反应中催化剂的用量并不是越多越好.
故答案为:(1)2KClO3
2KCl+3O2↑;
(2)1:10;
(3)MnO2与KClO3的接触面积小,因此催化作用不明显;
(4)质量分数;
(5)不是.
| ||
| △ |
(2)通过表格可知所需要的时间越短,反应的速度就越快,所以二氧化锰与氯酸钾的质量比为1:10时,反应速度最快;
(3)反应速度的影响因素主要是反应物的接触面积,接触面积越大反应速度就越快,二氧化锰的用量过少与氯酸钾的接触面积就越小,所以反应速度慢;
(4)二氧化锰用量过多氯酸钾的质量分数就降低了,反应物的接触面积就少了,就影响了反应速度;
(5)通过上面的表格显示的内容可知在化学反应中催化剂的用量并不是越多越好.
故答案为:(1)2KClO3
| ||
| △ |
(2)1:10;
(3)MnO2与KClO3的接触面积小,因此催化作用不明显;
(4)质量分数;
(5)不是.
点评:此题探究实验室用二氧化锰与氯酸钾制取氧气时,二氧化锰作催化剂的量要适中,过多或过少反应速率都或受到影响.希望同学们作此试验时注意二氧化锰的用量,节约药品.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
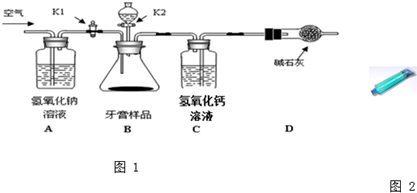 牙膏是生活中常见的物质,其配料成分有摩擦剂、增稠剂、发泡剂等,其中摩擦剂的类型有很多,如CaCO3、Al(OH)3、SiO2或这些物质的混合物.我校兴趣小组想研究牙膏摩擦剂的成分如图2.
牙膏是生活中常见的物质,其配料成分有摩擦剂、增稠剂、发泡剂等,其中摩擦剂的类型有很多,如CaCO3、Al(OH)3、SiO2或这些物质的混合物.我校兴趣小组想研究牙膏摩擦剂的成分如图2.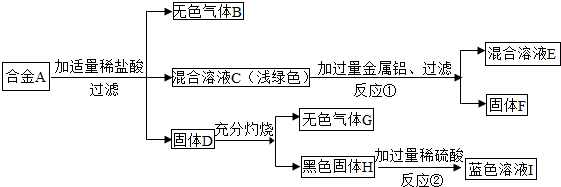
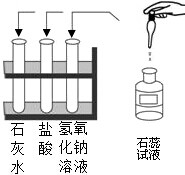 国家环保总局已规定将各类实验室纳入环保监管范围.某中学九年级A、B两个班的同学分别做常见酸、碱与指示剂反应的实验(如图所示),实验后溶液分别集中到各班的一个废液缸中.甲班的废液呈红色,乙班的废液呈蓝色.
国家环保总局已规定将各类实验室纳入环保监管范围.某中学九年级A、B两个班的同学分别做常见酸、碱与指示剂反应的实验(如图所示),实验后溶液分别集中到各班的一个废液缸中.甲班的废液呈红色,乙班的废液呈蓝色.