题目内容
【题目】氢氧化钠是一种重要的化工原料.
(1)氢氧化钠俗称 .
(2)利用如图所示装置(固定装置省略)进行NaOH与CO2气体反应的实验.若A与C连接,将分液漏斗中部分NaOH溶液注入烧瓶中,然后关闭活塞并打开止水夹,观察到的实验现象是;CO2与NaOH溶液反应的化学方程式是 . 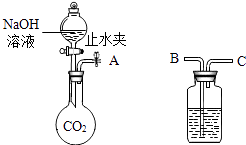
(3)已知:Na2CO3+H2O+CO2=2NaHCO3; NaHCO3+NaOH=Na2CO3+H2O 将(2)中实验后烧瓶内的溶液在低温下蒸干得到白色固体X,则X的组成可能有四种情况,分别是:
Ⅰ.NaOH,Na2CO3;Ⅱ.;Ⅲ.;Ⅳ.NaHCO3
(4)根据以上信息,请设计一种以100mL未知浓度的NaOH溶液和CO2气体为原料获得Na2CO3溶液的方法 .
【答案】
(1)火碱、烧碱、苛性钠
(2)B导管口产生气泡;2NaOH+CO2═Na2CO3+H2O
(3)Na2CO3、NaHCO3;Na2CO3
(4)先向100mL氢氧化钠溶液中通入过量的二氧化碳,再取100mL相同浓度的氢氧化钠溶液和生成的碳酸氢钠溶液混合
【解析】解:(1)氢氧化钠俗称火碱、烧碱、苛性钠. 故填:火碱、烧碱、苛性钠.(2)若A与C连接,将分液漏斗中部分NaOH溶液注入烧瓶中,然后关闭活塞并打开止水夹,由于二氧化碳被消耗后,会导致烧瓶中的压强减小,空气会通过B进入洗气瓶中,通过C进入烧瓶,因此能够观察到B导管口产生气泡;
CO2与NaOH溶液反应的化学方程式是:2NaOH+CO2═Na2CO3+H2O.
故填:B导管口产生气泡;2NaOH+CO2═Na2CO3+H2O.(3)二氧化碳和氢氧化钠反应时,如果氢氧化钠过量,则溶质是氢氧化钠和碳酸钠;
如果二氧化碳过量,但是不能完全消耗生成的碳酸钠,则溶质是碳酸钠和碳酸氢钠;如果氢氧化钠和二氧化碳恰好完全反应,则溶质是碳酸钠;
如果二氧化碳过量,并且把碳酸钠完全消耗,则溶质是碳酸氢钠.
故填:Na2CO3、NaHCO3;Na2CO3 . (4)以100mL未知浓度的NaOH溶液和CO2气体为原料获得Na2CO3溶液的方法是:先向50mL氢氧化钠溶液中通入过量的二氧化碳,再取50mL相同浓度的氢氧化钠溶液和生成的碳酸氢钠溶液混合.
故填:先向50mL氢氧化钠溶液中通入过量的二氧化碳,再取50mL相同浓度的氢氧化钠溶液和生成的碳酸氢钠溶液混合.
【考点精析】认真审题,首先需要了解书写化学方程式、文字表达式、电离方程式(注意:a、配平 b、条件 c、箭号).