题目内容
将X溶液分别加入AgNO3溶液、Na2CO3溶液,Na2SO4溶液中,反应均有白色沉淀,则X是
A.BaCl2 B.HCl C.Ca(NO3)2 D.NaOH
根据下表回答问题。
温度/℃ | 20 | 40 | 50 | 60 | 80 | |
溶解度/g | NaCl | 36.0 | 36.6 | 37.0 | 37.3 | 38.4 |
NH4Cl | 37.2 | 45.8 | 50.4 | 55.2 | 65.6 | |
KNO3 | 31.6 | 63.9 | 85.5 | 110 | 169 |
(1)20℃时,溶解度最大的物质是__________
(2)50℃时,在100g水中放入36g氯化钠充分溶解持温度降到40℃,得到的是氯化钠的溶液__________(选填“饱和”或“不饱和”):
(3)现将100gKNO3和38gNaCl同时放入一个盛有100克80℃水的烧杯中,然后降温至20℃,得到的溶液中,KNO3的溶质质量分数的计算式为__________。
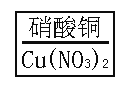
下列化学用语中“2”所表示的意义正确的是( )
A.2Al:两个氯原子 B.Fe2+:每个铁离子带两个单位的正电荷
C.CO2 :一个二氧化碳分子中含有两个氧分子 D. :在氧化镁中,镁元素的化合价为+2价
:在氧化镁中,镁元素的化合价为+2价
[观察与问题]镁条在空气中久置表面会变黑,某小组同学设计并进行实验,探究镁条变黑的条件。
I.从生成物角度分析,进行探究
实验一:刮下镁条表面的黑色物质于试管中,加入足量的稀盐酸产生气体,把生成的气体通入澄清石灰水,观察到石灰水变浑浊。由此可知镁条变黑与空气中的_________有关,原因是_________。
II.从反应物角度分析,进行探究
[猜想与假设]在实验一的基础上猜想镁条变黑具体与空气中的哪些物质有关,甲、乙、丙、丁四位同学分别提出了如下猜想:
甲: CO2
乙: CO2 O2
丙: CO2 H2O
丁:_________。
[实验与探究]
实验二:通过控制与镁条接触的物质,利用如图所示装置(镁条长度为3 cm,试管容积为20 mL),分别进行下列4个实验,并持续观察10天。请将下表中实验操作补充完整。
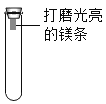
编号 | 主要实验操作 | 实验现象 |
① | 先收集满二氧化碳,再加入2ml浓硫酸 | 镁条始终无明显变化 |
② | 先集满体积比为1 : 1的二氧化碳和氧气的混合气体,再加 入__________ mL浓硫酸 | 镁条始终无明显变化 |
③ | 先收集满二氧化碳,再加入2mL蒸馏水 | 镁条始终无明显变化 |
④ | 先集满体积比为1 : 1的二氧化碳和氧气的混合气体,再加入2 mL蒸馏水 | 镁条第1天开始变黑至第10天全部变黑 |
[解释与结论]
(1)实验①和②中的浓硫酸的作用是___________。在这两个实验中____________(填“能”或“不能”)用烧碱代替浓硫酸,原因是_____________(用化学方程式表示)。
(2)实验③的目的__________。
(3)由上述实验可推知,镁条变黑的条件是________。
[反思与评价]
(4)在猜想与假设时,同学们认为镁条变黑与N2无关,其理由是__________。




 B.
B.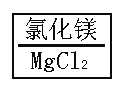 C.
C.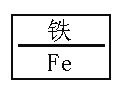 D.
D.