题目内容
甲烷在一定量的氧气中燃烧,测得反应前后各物质的质量如下表所示:
下列判断正确的是
A.表中a的值为2.6 B.X一定是该反应的催化剂
C.X可能含有氢元素 D.X一定含有氧元素
| 物质 | 甲烷 | 氧气 | 水 | 二氧化碳 | X |
| 反应前质量/g | 3.2 | 11.2 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 7.2 | 4.4 | a |
A.表中a的值为2.6 B.X一定是该反应的催化剂
C.X可能含有氢元素 D.X一定含有氧元素
D
试题分析:根据质量守恒定律分析。
A、由质量守恒定律可知,反应前物质质量总和=反应后物质质量总和,故3.2g+11.2g=7.2g+4.4g+a,解得a=2.8g,错误;
B、由于X的质量在反应后增加,故说明X为生成物,错误;
C、反应物中3.2g甲烷含氢元素的质量=3.2g×
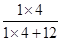 ×100%=0.8g,而生成物中7.2g水含氢元素的质量=7.2g×
×100%=0.8g,而生成物中7.2g水含氢元素的质量=7.2g×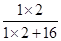 ×100%=0.8g,由此可知,生成物X中不含有氢元素,错误;
×100%=0.8g,由此可知,生成物X中不含有氢元素,错误;D、根据C中的计算可知,3.2g甲烷中的碳元素的质量=3.2g-0.8g=2.4g,而4.4g二氧化碳中碳元素的质量=4.4g×
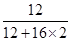 ×100%=1.2g,故X中应含有2.4g-1.2g=1.2g碳元素,又因为X的质量是2.8g,故X中应含有1.6g氧元素,正确。故选D
×100%=1.2g,故X中应含有2.4g-1.2g=1.2g碳元素,又因为X的质量是2.8g,故X中应含有1.6g氧元素,正确。故选D点评:理解和熟记质量守恒定律及其应用,以及与之相关的知识,特别是化学变化中的元素守恒的知识,是解题的关键。

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目