题目内容
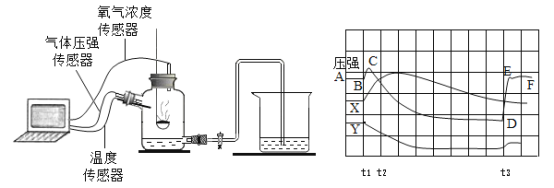
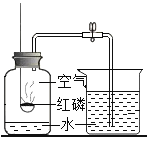
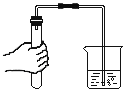
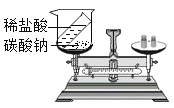
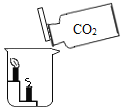
【题目】某化学兴趣小组用如图所示的实验装置,探究影响过氧化氢分解速率的因素。

(1)写出过氧化氢分解的化学方程式 ;装置中使用注射器的优点是 。
(2)下面是用上述装置实验时,收集的相关数据:
实验 序号 | H2O2溶液浓度/% | 体积/mL | MnO2的量/g | 温度/℃ | 收集的体积/mL | 反应所需的时间/s |
① | 5 | 2 | 0.1 | 20 | 4 | 18 |
② | 10 | 2 | 0.1 | 20 | 4 | 6 |
③ | 5 | 2 | / | 20 | 4 | 64 |
④ | 5 | 2 | / | 60 | 4 | 25 |
从实验①和②对比可知,化学反应速率与 有关;
从实验③和④对比可知,化学反应速率与 有关;
从实验对比可知,化学反应速率是否加MnO2有关。
(3)发现问题:实验温度最难控制,反应一段时间后溶液的温度总是比起始温度高,说明反应 (填“放出”或“吸收”)热量
(4)继续探究:除了该实验小组探究过的因素以外,你若还有其他影响反应速率的因素及探究方法,请写在下面。
【答案】2H2O2![]() 2H2O+O2↑ 可控制过氧化氢溶液的使用量 反应物浓度 温度 ①③ 放出(4)催化剂种类;20℃时,分别取2mL5%过氧化氢溶液于两支试管中,一支试管中加入0.1g二氧化锰粉末,另一支试管中加入0.1g颗粒大小相同的氧化铁粉末,分别收集4mL氧气,记录反应所需时间。(另有催化剂颗粒大小等因素,答案合理即可)
2H2O+O2↑ 可控制过氧化氢溶液的使用量 反应物浓度 温度 ①③ 放出(4)催化剂种类;20℃时,分别取2mL5%过氧化氢溶液于两支试管中,一支试管中加入0.1g二氧化锰粉末,另一支试管中加入0.1g颗粒大小相同的氧化铁粉末,分别收集4mL氧气,记录反应所需时间。(另有催化剂颗粒大小等因素,答案合理即可)
【解析】
试题分析:(1)过氧化氢分解的化学方程式为2H2O2![]() 2H2O+O2↑,装置中使用注射器的优点是可控制过氧化氢溶液的使用量及反映速率;(2)从实验①和②对比可知,化学反应速率反应物浓度与有关;从实验③和④对比可知,化学反应速率与温度有关;(3)发现问题:实验温度最难控制,反应一段时间后溶液的温度总是比起始温度高,说明反应放出热量;(4)催化剂种类;20℃时,分别取2mL5%过氧化氢溶液于两支试管中,一支试管中加入0.1g二氧化锰粉末,另一支试管中加入0.1g颗粒大小相同的氧化铁粉末,分别收集4mL氧气,记录反应所需时间。(另有催化剂颗粒大小等因素,答案合理即可)
2H2O+O2↑,装置中使用注射器的优点是可控制过氧化氢溶液的使用量及反映速率;(2)从实验①和②对比可知,化学反应速率反应物浓度与有关;从实验③和④对比可知,化学反应速率与温度有关;(3)发现问题:实验温度最难控制,反应一段时间后溶液的温度总是比起始温度高,说明反应放出热量;(4)催化剂种类;20℃时,分别取2mL5%过氧化氢溶液于两支试管中,一支试管中加入0.1g二氧化锰粉末,另一支试管中加入0.1g颗粒大小相同的氧化铁粉末,分别收集4mL氧气,记录反应所需时间。(另有催化剂颗粒大小等因素,答案合理即可)

【题目】钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量。某补钙药剂主要成分为碳酸钙,现将100g盐酸分成5等份,逐次加到用10g该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图象,请根据有关信息回答问题:
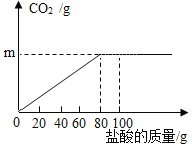
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
加入盐酸的质量(g) | 20 | 20 | 20 | 20 | 20 |
生成气体的质量(g) | 0.6 | 1.2 | 1.8 | 2.2 | a |
(1)求碳酸钙中各元素的质量比Ca:C:O=______。(化成最简整数比)
(2)a的数值为______。
(3)求该品牌补钙药剂中CaCO3的质量分数____(写出计算过程,计算结果保留一位小数)。