题目内容
【题目】如图为某学习小组探究金属化学性质时所做的四个实验,仔细分析后回答下列问题: 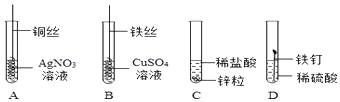
(1)描述A中的实验现象 .
(2)写出C中反应的化学方程式 .
(3)要证明Cu、Fe、Ag的活动性顺序,至少要做的实验是(填序号).
(4)开始反应后D中溶液逐渐变为黄色,原因是 , 写出反应的化学方程式 .
【答案】
(1)铜丝表面附着一层银白色固体,溶液变为蓝色
(2)Zn+2HCl═ZnCl2+H2↑
(3)A、B
(4)铁钉表面有铁锈,铁锈与稀硫酸反应生成硫酸铁,从而是溶液变黄;Fe2O3+3H2SO4=3H2O+Fe2(SO4)3
【解析】解:(1)由于在金属活动性顺序中铜>银,所以铜可以置换出银,并生成蓝色的硝酸铜溶液,所以其现象是:铜丝表面附着一层银白色固体,溶液变为蓝色;(2)C中是锌与稀盐酸的反应,锌的活动性在氢的前面,所以锌与稀盐酸可以反应生成氢气,其反应的方程式为:Zn+2HCl═ZnCl2+H2↑;(3)用于证明铁、铜、银的金属活动性顺序实验是A、B,因为由A知铜能置换出硝酸银中的银,说明活动性铜>银,B中的铁能置换出硫酸铜中的铜,说明活动性铁>铜,所以可得活动性:铁>铜>银;(4)从变黄色可推测溶液中含有铁离子,所以可猜想是铁钉表面有铁锈,铁锈的主要成分是氧化铁,所以会与稀硫酸反应生成硫酸铁,从而是溶液变黄,化学方程式为:Fe2O3+3H2SO4=3H2O+Fe2(SO4)3 . 故答案为:(1)铜丝表面附着一层银白色固体,溶液变为蓝色;(2)Zn+2HCl═ZnC12+H2↑;(3)A、B;(4)铁钉表面有铁锈,铁锈与稀硫酸反应生成硫酸铁,从而是溶液变黄,Fe2O3+3H2SO4=3H2O+Fe2(SO4)3 .
根据在金属活动性顺序中,只有排在氢前的金属可以和稀酸溶液(除稀硝酸外)生成氢气,只有前面的金属可以把排在它后面的金属从盐溶液中置换出来,利用这一规律对问题进行判断分析即可.