题目内容
【题目】如图为两种物质在不同温度时的溶解度曲线.请回答: 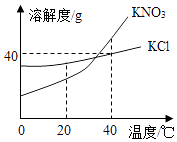
(1)40℃时,将30g KCl加入到50g水中,充分溶解后所得溶液是溶液(填写“饱和”或“不饱和”);
(2)将20℃时KNO3和KCl的两种饱和溶液升温至40℃,则两种溶液的溶质质量分数大小关系是:KNO3KCl(填写“>”、“<”或“=”).
【答案】
(1)饱和
(2)<
【解析】解:(1)由KCl的溶解度曲线可知,在40℃时,KCl的溶解度是40g,由溶解度的含义可知,40℃时,将30g KCl加入到50g水中,充分溶解,只能溶解20g,所得溶液是饱和溶液;(2)由两种物质的溶解度曲线可知,KNO3和KCl的溶解度都随温度的升高而增大,将20℃时KNO3和KCl的两种饱和溶液升温至40℃,都变成了不饱和溶液,溶质的质量分数不变,都等于将20℃时饱和溶液的质量分数,由于在20℃时KCl的溶解度大于KNO3的溶解度,所以两种溶液的溶质质量分数大小关系是:KNO3<KCl.
所以答案是:(1)饱和;(2)<.
【考点精析】通过灵活运用固体溶解度曲线及其作用和溶质的质量分数、溶解性和溶解度的关系,掌握1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性.2.比较相同温度时(或一定温度范围内)不同物质溶解度的大小.3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法.4.确定溶液的状态(饱和与不饱和);溶质质量分数 =溶质质量/溶液质量*100% ;溶解度=溶质质量/溶剂质量*100g (必须选取饱和溶液);溶液质量=溶质质量(克)+溶剂质量(克) ;对于饱和溶液,溶液质量分数w = S/(S+100);所以溶解度S = 100/(1/w-1)即可以解答此题.

 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案【题目】除去下列物质中的少量杂质(括号内为杂质)所用除去杂质的方法正确的是( )
选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
A | NaNO3溶液(NaCl) | 过量的AgNO3溶液 | 过滤 |
B | H2O(臭味物质) | 足量活性炭 | 吸附 |
C | CO(H2O) | 足量的浓硫酸 | 洗气 |
D | CuSO4(Fe) | 足量水 | 溶解、过滤、洗涤、干燥 |
A.AB.BC.CD.D