题目内容
浩瀚无际的海洋为人类提供了丰富的资源.由海水制备金属镁,主要有以下步骤:(1)电解熔融的氯化镁(MgCl2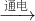 Mg+Cl2↑);(2)加熟石灰;(3)加盐酸;(4)过滤;(5)浓缩结晶.其先后顺序正确的是
Mg+Cl2↑);(2)加熟石灰;(3)加盐酸;(4)过滤;(5)浓缩结晶.其先后顺序正确的是
- A.(2)(4)(5)(3)(1)
- B.(3)(2)(4)(1)(5)
- C.(3)(4)(2)(5)(1)
- D.(2)(4)(3)(5)(1)
D
分析:由于海水含有大量的氯化镁,因此常用海水来制备金属镁,大体步骤为:将石灰乳加入海水或卤水中,沉淀出氢氧化镁,氢氧化镁再和稀盐酸反应生成氯化镁,然后对得到的氯化镁溶液蒸发结晶,电解熔融状态的氯化镁,就能得到金属镁.
解答:根据题意提供的五个步骤采用逆推法分析:
最后一步应该是(1)电解熔融的氯化镁MgCl2 Mg+Cl2↑;
Mg+Cl2↑;
再往前一步应该是制备熔融的氯化镁,分析应该是(5)浓缩结晶;
再往前一步应该是制备氯化镁溶液了,Mg(OH)2+2HCl=MgCl2+2H2O,分析应该是(3);
再往前一步应该是过滤得到氢氧化镁沉淀.
第一步应该是将海水的中镁离子富集起来,常用个的方法是沉淀,应该是(2)MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2;所以顺序应该选D.
故选D.
点评:本题难度不大,主要考查了海水制镁的过程,培养学生解决问题的能力,更全面地了解分离混合物的方法.
分析:由于海水含有大量的氯化镁,因此常用海水来制备金属镁,大体步骤为:将石灰乳加入海水或卤水中,沉淀出氢氧化镁,氢氧化镁再和稀盐酸反应生成氯化镁,然后对得到的氯化镁溶液蒸发结晶,电解熔融状态的氯化镁,就能得到金属镁.
解答:根据题意提供的五个步骤采用逆推法分析:
最后一步应该是(1)电解熔融的氯化镁MgCl2
 Mg+Cl2↑;
Mg+Cl2↑;再往前一步应该是制备熔融的氯化镁,分析应该是(5)浓缩结晶;
再往前一步应该是制备氯化镁溶液了,Mg(OH)2+2HCl=MgCl2+2H2O,分析应该是(3);
再往前一步应该是过滤得到氢氧化镁沉淀.
第一步应该是将海水的中镁离子富集起来,常用个的方法是沉淀,应该是(2)MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2;所以顺序应该选D.
故选D.
点评:本题难度不大,主要考查了海水制镁的过程,培养学生解决问题的能力,更全面地了解分离混合物的方法.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案
相关题目
浩瀚无际的海洋为人类提供了丰富的资源.由海水制备金属镁,主要有以下步骤:①电解熔融的氯化镁;②加熟石灰;③加盐酸;④过滤;⑤浓缩结晶.其先后顺序正确的是( )
| A、②④⑤③① | B、③②④①⑤ | C、③④②⑤① | D、②④③⑤① |
浩瀚无际的海洋为人类提供了丰富的资源.由海水制备金属镁,主要有以下步骤:(1)电解熔融的氯化镁(MgCl2
Mg+Cl2↑);(2)加熟石灰;(3)加盐酸;(4)过滤;(5)浓缩结晶.其先后顺序正确的是( )
| 通电 |
| A、(2)(4)(5)(3)(1) |
| B、(3)(2)(4)(1)(5) |
| C、(3)(4)(2)(5)(1) |
| D、(2)(4)(3)(5)(1) |
 Mg+Cl2↑);(2)加熟石灰;(3)加盐酸;(4)过滤;(5)浓缩结晶.其先后顺序正确的是( )
Mg+Cl2↑);(2)加熟石灰;(3)加盐酸;(4)过滤;(5)浓缩结晶.其先后顺序正确的是( )