题目内容
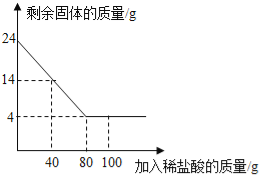
【题目】某化学兴趣小组为了测定当地的石灰石(主要成分是CaCO3)的质量分数,他们做了如下实验:取24克样品放入烧杯中,向其中逐渐加入100克一定质量分数的稀盐酸(杂质不溶于水也不与酸反应),所用盐酸的质量分数与剩余固体的质量关系如图所示,请根据图中的数据进行计算:
(1)石灰石样品中CaCO3的质量为 克.
(2)24克石灰石样品与盐酸充分反应后最多产生二氧化碳的质量为 克.
(3)求所用盐酸的溶质质量分数.(请根据化学方程式写出完整的计算步骤)
【答案】(1)20;(2)8.8;(3)所用盐酸的溶质质量分数为:18.25%
【解析】试题分析:(1)由图象可知最终反应后固体的固体为4g,该质量即是剩余的不反应的杂质的质量,所以石灰石中碳酸钙的质量是24g﹣4g=20g;
(2)由图象可知碳酸钙与盐酸恰好反应时的用量是80g;
解:设参加反应的盐酸中HCl的质量为x.生成的二氧化碳的质量是y
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
20g x y
![]()
x=14.6g y=8.8g
(3)由图象可知碳酸钙与盐酸恰好反应时的用量是80g;所以所用盐酸的质量分数为![]() ×100%=18.25%
×100%=18.25%

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
【题目】下列四个实验方案设计不合理的是
选项 | 实验目的 | 实验方案 |
A | 鉴别氯化铵和尿素 | 分别加熟石灰粉末研磨,闻气味 |
B | 鉴别硝酸铵和氯化钠 | 分别加适量水,用手触摸容器壁 |
C | 鉴别硫酸铜溶液和稀盐酸 | 分别观察溶液颜色 |
D | 鉴别烧碱溶液和石灰水 | 分别滴加酚酞试液,观察颜色变化 |
A. A B. B C. C D. D
