题目内容
【题目】(6分)在宏观、微观和符号之间建立联系是化学学科的特点。
(1)硫酸铜、汞、氢气三种物质中,由原子构成的是(写化学式) 。
(2)下图表示核电荷数为11~17的元素最高和最低化合价。
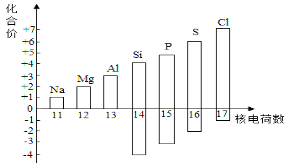
①硫元素的最高正价氧化物的化学式为 。
②若某元素既可显正价,又可显负价,则最高正价与最低负价绝对值的代数和为 。
(3)在点燃条件下,A和B反应生成C和D。反应前后分子变化的微观示意图如下所示。

①该反应的基本反应类型为 。
②该反应中A、C两种物质的质量比为 。
(4)下图表示氢氧化钠溶液与稀盐酸反应的微观过程。
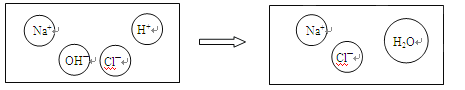
请你在下图圆圈中处将BaCl2溶液和CuSO4溶液反应的产物补充完整:

【答案】(1)Hg
(2)① SO3 ②8
(3)① 置换反应 ② 17:14
(4)BaSO4
【解析】
试题分析:(1)硫酸铜属于盐,由离子构成,汞属于金属,直接由原子构成,氢气是气态非金属单质,由分子构成,故三种物质中,由原子构成的是Hg
(2)①硫元素的最高正价为+6,氧元素的化合价为-2,故氧化物的化学式为SO3
②根据图示:若某元素既可显正价,又可显负价,则最高正价与最低负价绝对值的代数和为8
(3)①通过观察微观示意图,该反应是一种单质和一种化合物生成另一种单质和一中化合物,故基本反应类型为置换反应
②根据变化的微观示意图,可书写化学方程式为:4NH3+3O2点燃2N2+6H2O,该反应中A、C两种物质的质量比为17:14
(4)通过观察氢氧化钠溶液与稀盐酸反应的微观过程,实际就是离子间的相互结合形成沉淀、气体或水故BaCl2溶液和CuSO4溶液实际发生反应的离子是Ba2+和SO42-两者结合的产物是BaSO4

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目