题目内容
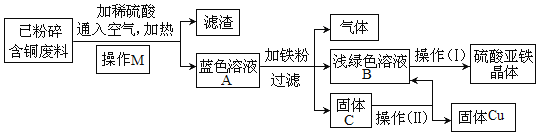
【题目】电缆的生产过程中会产生一定量的含铜废料。某化学兴趣小组同学按下列方案分离回收铜,并获得硫酸亚铁晶体。
(查阅资料)
①在通入空气并加热的条件下,铜可与稀硫酸反应转化为硫酸铜。反应的化学方程式:2Cu + 2H2SO4 + O2 ![]() 2CuSO4 + 2H2O。
2CuSO4 + 2H2O。
②硫酸亚铁的溶解度随着温度升高而增大(在一定温度范围内)。
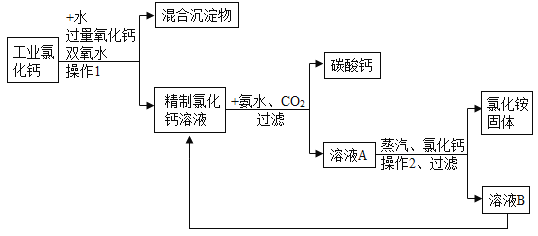
(1)操作M名称是_______。
(2)蓝色溶液A中溶质的成分是________(填化学式)。
(3)浅绿色溶液B经系列操作(I)可得硫酸亚铁晶体(FeSO4·7H2O),该操作的顺序为_____(用a、b、c 表示)。
a.冷却结晶 b.过滤 c.加热浓缩
(4)该方案中应该加入略过量的铁粉,铁粉过量的目的是________;从固体C 中获得纯净的铜,操作(Ⅱ)的具体处理方法是:加入_________充分反应后过滤、洗涤、干燥。
【答案】过滤 CuSO4 、H2SO4 c→a→b 将Cu完全置换出来 稀硫酸
【解析】
(1)操作M实现了固液分离,故操作M的名称是:过滤;
(2)在通入空气并加热的条件下,铜可与稀硫酸反应转化为硫酸铜,向蓝色溶液A中加铁粉,有气体产生,说明蓝色溶液A中含有稀硫酸,铁与稀硫酸反应生成了氢气,故蓝色溶液A中溶质的成分是:CuSO4 、H2SO4;
(3)浅绿色溶液B为铁与硫酸反应生成的硫酸亚铁溶液,由溶液得到硫酸亚铁晶体,需要蒸发浓缩、降温结晶、过滤,该操作的顺序为:c→a→b;
(4)铁能与硫酸铜反应生成硫酸亚铁和铜,加入过量的铁粉,铁可将铜完全置换出来;
固体C中含有铜和过量的铁,可加入稀硫酸,使铁与稀硫酸反应生成硫酸亚铁和氢气,过滤、洗涤、干燥,得到铜,故填:将铜完全置换出来,稀硫酸。

 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
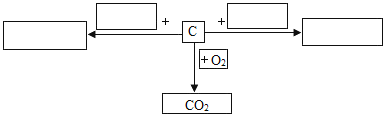
步步高口算题卡系列答案【题目】(1)一定条件下碳能跟很多物质发生反应。以碳为研究对象,仿照下图中实例,在框格中填写物质的化学式,完成有关碳的化学性质的网络图(产物要全部写出)。____
(2)石灰石、生石灰和熟石灰在日常生活中有多种用途,请在下表中写出有关的化学方程式,并回答有关的问题:
用途 | 化学方程式 | 相关问题 |
用石灰石制生石灰 | _____ | 反应类型_____ |
生石灰常用作某些食品的干燥剂 | ____ | 此反应_____(填“吸收”或“放热”) |