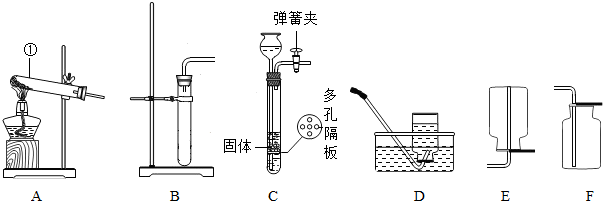
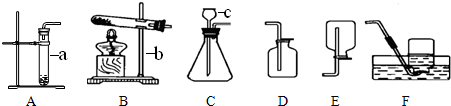
题目内容
实验室用过氧化氢溶液(过氧化氢与水的混合物)制取氧气.某同学实验前称得过氧化氢溶液42.5克,加入1克二氧化锰,完全反应后称得剩下的固体与液体的总质量为41.9克,计算:
(1)反应中放出氧气的质量?
(2)实验中加入的过氧化氢溶液中过氧化氢的质量?
(1)反应中放出氧气的质量?
(2)实验中加入的过氧化氢溶液中过氧化氢的质量?
分析:首先根据质量守恒定律利用物质的总质量的减少得出生成的气体的质量,然后把生成的气体的质量代入化学方程式进行计算.
解答:解:(1)氧气的质量:42.5g+1g-41.9g=1.6g
(2)设:过氧化氢溶液中过氧化氢的质量为x
2H2O2
2H2O+O2↑
68 32
x 1.6g
=
x=3.4g
答:(1)反应中放出氧气的质量是1.6g;(2)实验中加入的过氧化氢溶液中过氧化氢的质量是3.4g.
(2)设:过氧化氢溶液中过氧化氢的质量为x
2H2O2
| ||
68 32
x 1.6g
| 68 |
| 32 |
| x |
| 1.6g |
x=3.4g
答:(1)反应中放出氧气的质量是1.6g;(2)实验中加入的过氧化氢溶液中过氧化氢的质量是3.4g.
点评:本题难度不大,主要考查了根据化学方程式来计算有关的量,从而使学生来认识化学反应的本质,计算时要注意代入化学方程式计算的数据必须是纯净物的质量才行.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目