题目内容
(2009?北京)甲是初中化学中的常见物质.请根据下列叙述回答问题.
(1)若甲能与稀硫酸反应生成一种在标准状况下密度最小的气体,该气体的化学式为:
(2)若甲是一种红色的氧化物,能溶于稀盐酸,得到黄色溶液,则甲的化学式为
(3)若甲既能与稀盐酸反应生成X,又能与氢氧化钙溶液反应生成Y,且X与Y能反应.则甲的化学式可能是
(4)若甲能与水反应,将少量甲加到饱和石灰水中,溶液变浑浊,则下列说法正确的是
A、甲一定是二氧化碳
B、反应后溶质的质量一定减少
C、反应前后溶剂的质量保持不变
D、反应前后溶液中溶质的质量分数可能不变.
(1)若甲能与稀硫酸反应生成一种在标准状况下密度最小的气体,该气体的化学式为:
H2
H2
,甲在常见的金属活动性顺序中的位置是H之前的金属
H之前的金属
.(2)若甲是一种红色的氧化物,能溶于稀盐酸,得到黄色溶液,则甲的化学式为
Fe2O3
Fe2O3
.(3)若甲既能与稀盐酸反应生成X,又能与氢氧化钙溶液反应生成Y,且X与Y能反应.则甲的化学式可能是
Na2CO3
Na2CO3
(写出一种既可),X与Y反应的化学方程式为2NaOH+CO2=Na2CO3+H2O
2NaOH+CO2=Na2CO3+H2O
.(4)若甲能与水反应,将少量甲加到饱和石灰水中,溶液变浑浊,则下列说法正确的是
B、D
B、D
(填字母序号)A、甲一定是二氧化碳
B、反应后溶质的质量一定减少
C、反应前后溶剂的质量保持不变
D、反应前后溶液中溶质的质量分数可能不变.
分析:(1)根据密度的大小和气体的相对分子质量有关进行分析,根据金属活动顺序表解答.
(2)根据物质的颜色红色氧化物,溶液的颜色黄色,存在铁离子进行猜想分析,
(3)甲既能与稀盐酸反应生成X,又能与氢氧化钙溶液反应生成Y,能和酸反应,又能和碱反应,所以甲是可溶性盐,x和y会反应,根据复分解反应的原理,所以y是可溶性碱,甲就是碳酸盐,
(4)根据题中的现象可知,甲可能是二氧化碳,氢氧化钙的溶解度随温度的升高而减小,在饱和的石灰水中加氧化钙,会使溶液温度升高,也可能是氧化钙,
(2)根据物质的颜色红色氧化物,溶液的颜色黄色,存在铁离子进行猜想分析,
(3)甲既能与稀盐酸反应生成X,又能与氢氧化钙溶液反应生成Y,能和酸反应,又能和碱反应,所以甲是可溶性盐,x和y会反应,根据复分解反应的原理,所以y是可溶性碱,甲就是碳酸盐,
(4)根据题中的现象可知,甲可能是二氧化碳,氢氧化钙的溶解度随温度的升高而减小,在饱和的石灰水中加氧化钙,会使溶液温度升高,也可能是氧化钙,
解答:解:(1)气体的密度和相对分子质量的大小成正比,气体的密度最小,其相对分子质量最小,所以只有氢气,故答案为:H2,
能够将硫酸中的氢置换出来,金属的活动性必须位于氢之前,故答案为:H之前的金属,
(2)红色氧化物与盐酸反应会生成三价铁的溶液,只能是氧化铁,故答案为:Fe2O3,
(3)甲既能与稀盐酸反应生成X,又能与氢氧化钙溶液反应生成Y,能和酸反应,又能和碱反应,所以甲是可溶性盐,x和y会反应,y是可溶性碱,甲就是碳酸盐,
故答案为:Na2CO3,2NaOH+CO2=Na2CO3+H2O,
(4)石灰水中通入二氧化碳会出现浑浊,但是饱和的石灰水中,加入氧化钙会消耗水分,溶剂减少,氢氧化钙会从溶液中析出,会使溶液的溶质减少,只要温度不变,溶质的质量分数就不变,故选BD.
能够将硫酸中的氢置换出来,金属的活动性必须位于氢之前,故答案为:H之前的金属,
(2)红色氧化物与盐酸反应会生成三价铁的溶液,只能是氧化铁,故答案为:Fe2O3,
(3)甲既能与稀盐酸反应生成X,又能与氢氧化钙溶液反应生成Y,能和酸反应,又能和碱反应,所以甲是可溶性盐,x和y会反应,y是可溶性碱,甲就是碳酸盐,
故答案为:Na2CO3,2NaOH+CO2=Na2CO3+H2O,
(4)石灰水中通入二氧化碳会出现浑浊,但是饱和的石灰水中,加入氧化钙会消耗水分,溶剂减少,氢氧化钙会从溶液中析出,会使溶液的溶质减少,只要温度不变,溶质的质量分数就不变,故选BD.
点评:在做物质的推断题时,先根据特殊的现象进行猜想,然后进行验证即可.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
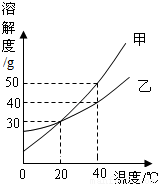
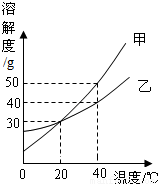
 (2009?北京)甲、乙两种固体的溶解度曲线如图所示,下列说法中,正确的是( )
(2009?北京)甲、乙两种固体的溶解度曲线如图所示,下列说法中,正确的是( )