题目内容
【题目】下表是元素周期表的部分信息(左下角数字表示相应元素的原子序数)。
1H | |||||||
6C | 7N | 8O | 9F | ||||
12Mg | 13Al | 14Si | 17Cl | ||||
(1)上述元素中属于金属元素的有_____种,决定不同元素的最本质的区别是______不同。
(2)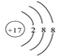 表示的是______(写微粒符号)。
表示的是______(写微粒符号)。
(3)地壳中含量最多的金属元素与海水中含量最多的元素组成的化合物的化学式是______,其中显正价的元素的化合价为______。
【答案】 2 核电荷数(质子数) Cl- Al2O3 +3
【解析】(1)上述元素中属于金属元素的有镁和铝两种;质子数不同元素的种类也不同,所以决定不同元素的最本质的区别是质子数不同;(2) 的核外电子数为2+8+8=18>17,得到一个电子,带一个单位的负电荷,17号元素是氯元素,所以离子符号为:Cl-;(3)地壳中含量最多的金属元素铝元素,海水中含量最多的元素是氧元素,它们组成的化合物的化学式是Al2O3 ,铝显正价,化合价为+3价。
的核外电子数为2+8+8=18>17,得到一个电子,带一个单位的负电荷,17号元素是氯元素,所以离子符号为:Cl-;(3)地壳中含量最多的金属元素铝元素,海水中含量最多的元素是氧元素,它们组成的化合物的化学式是Al2O3 ,铝显正价,化合价为+3价。

 科学实验活动册系列答案
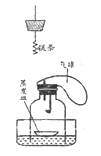
科学实验活动册系列答案【题目】某科学兴趣小组如下图所示装置测定空气中氧气含量,并对剩余的氮气产生了兴趣。查阅资料得知镁可在氧气中燃烧生成氧化镁,镁可在氮气中燃烧生成氮化镁(Mg3N2),设计了如下方案进行验证。
实验装置如图:用盛水的水槽、无底的废广口瓶、燃烧匙、蒸发皿、橡皮塞等装配成如图所示的装置。蒸发皿浮在水面上。
实验装置 | 【实验1】测定氧气含量. | 【实验2】验证氮气 |
| I. 引燃燃烧匙中足量的红磷,塞好橡皮塞。 待充分冷却,观察到广口瓶内水面上升的体积约占瓶内水面原上方空间的1/5左右。 II. 往水槽中加水使广口瓶内外水面相平。 | I. 继续【实验1】,更换燃烧下端系镁条的燃烧匙,并点燃镁条。 镁条在广口瓶内继续燃烧,发出红光,蒸发皿中出现淡黄色固体。待冷却后广口瓶内水位继续上升。 II. 取出蒸发皿,滴入几滴水,淡黄色固体变白,闻到刺激性气味气体。 |
(1)连接仪器后,把组装好的无底广口瓶直接压入水槽当中,气球微微鼓起并保持,该现象说明___________。
(2)【实验1】除上表中描述的现象之外,还会观察到的现象为__________;步骤II的目的是______________。
(3)【实验2】中广口瓶内水位继续上升过程中瓶内气压______________(选填“大于”“小于”或“等于”)外界气压。
(4)【反思】同学们在空气中直接燃烧镁条,重复多次仍然未能得到淡黄色固体。与上述实验对比,对此请你给出合理解释__________。

请补充完成【实验2】中步骤II的反应方程式Mg3N2+6H2O==3Mg(OH)2 +2_________。