题目内容
【题目】下列各组元素的原子结构示意图中,具有相似化学性质的一组元素是( )
A. 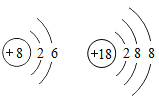 B.
B. 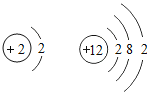
C. 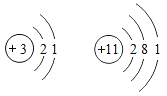 D.
D. 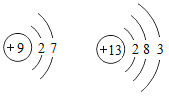
【答案】C
【解析】
A、质子数为8的原子最外层电子数为6,易得2个电子形成稳定结构;质子数为18的原子,最外层电子达8电子稳定结构,性质稳定,化学性质不同,故A错误;
B、虽然两种元素的原子的最外层电子数相同,但它们的化学性质却完全不同。质子数为2的为稀有气体元素的原子,化学性质稳定;质子数为12的原子最外层电子数为2,易失最外层的2个电子形成稳定结构,化学性质不同,故B错误;
C、两种原子的最外层电子数均为1,最外层电子数相同,具有相似化学性质,故C正确;
D、两种原子的最外层电子数分别为7、3,最外层电子数不同,化学性质不相似,故D错误。故选C。

练习册系列答案
相关题目
【题目】工业中合成SO3的反应:2SO2+O2![]() 2SO3。一定条件下,在一密闭容器内投入 SO2、O2、SO3、V2O5四种物质,在不同时刻测得各物质的质量(单位为 g)如下表所示。说法错误的是
2SO3。一定条件下,在一密闭容器内投入 SO2、O2、SO3、V2O5四种物质,在不同时刻测得各物质的质量(单位为 g)如下表所示。说法错误的是
甲 | 乙 | 丙 | 丁 | |
t1 | 100 | 5 | 80 | 5 |
t2 | 60 | 55 | a | b |
t3 | 40 | c | d | 5 |
A.丁物质一定是V2O5
B.d=15
C.丙物质是O2
D.t3时,生成乙75g