题目内容
某化合物的化学式是H2ROn,已知该化合物中R的化合价为+6价,则n的值是
- A.1
- B.2
- C.3
- D.4
D
分析:根据物质的化学式为H2ROn,利用各种元素的化合价及化合物中各元素正负化合价的代数和为零列式计算得出n的数值.
解答:在H2ROn中,氢元素的化合价是+1价,氧元素的化合价是-2价,R的化合价为+6价,根据化合物中各元素正负化合价代数和为零的原则有(+1)×2+(+6)×1+(-2)×n=0,解得,n=4.
故选D.
点评:解答本题要理解在化合物中各元素正负化合价的代数和为零的原则,难度不大.
分析:根据物质的化学式为H2ROn,利用各种元素的化合价及化合物中各元素正负化合价的代数和为零列式计算得出n的数值.
解答:在H2ROn中,氢元素的化合价是+1价,氧元素的化合价是-2价,R的化合价为+6价,根据化合物中各元素正负化合价代数和为零的原则有(+1)×2+(+6)×1+(-2)×n=0,解得,n=4.
故选D.
点评:解答本题要理解在化合物中各元素正负化合价的代数和为零的原则,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某化合物中H、S两元素的化合价为+1、-2,该化合物的化学式是
A. | B. | C.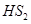 | D. |
(6分)下表是元素周期表的一部分:
|
族 周期 |
IA |
|
0 |
|||||
|
一 |
1 H 1.008 |
ⅡA |
ⅢA |
ⅣA |
V A |
ⅥA |
ⅦA |
2 He 4.003 |
|
二 |
3 Li 6.941 |
4 Be 9.012 |
5 B 10.81 |
6 C 12.01 |
7 N 14.01 |
8 O 16.00 |
9 F 19.00 |
10 Ne 20.18 |
|
三 |
11 Na 22.99 |
12 Mg 24.31 |
13 Al 26.98 |
14 Si 28.09 |
15 P 30.97 |
16 S 32.06 |
17 Cl 35.45 |
18 Ar 39.95 |
(1)Ne元素的原子核电荷数为_______,形成单质的化学式是 。
(2)某元素的原子结构示意图如右,则X的值为 。该元素与17号元素形成的化合物的化学式是 ,化合物中阴离子的结构示意图是 。

(3)请用表中的元素符号所组成的反应物写出符合要求的化学方程式:有水生成的化合反应:________________________________________。
 如图为某化合物的分子模型,该化合物是一种高效食品防腐剂.下列说法不正确的是( )
如图为某化合物的分子模型,该化合物是一种高效食品防腐剂.下列说法不正确的是( )