��Ŀ����
����Ŀ��С�ͻ��������Դ���ʹ���ʯΪ��Ҫԭ�ϣ������¹������������ռNaOH����

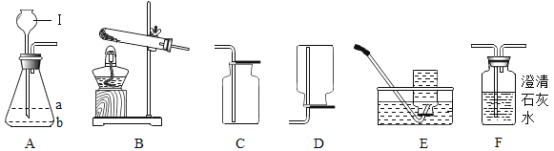
��1������C�Ļ�ѧʽ��_____���ڲ������Ҫ���еķ��������_____��
��2��д�������Ļ�ѧ����ʽ��_____��
��3��д�������Ļ�ѧ����ʽ��_____��
���𰸡�Ca��OH��2 ���� CaCO3![]() CaO+CO2�� Ca��OH��2+Na2CO3��CaCO3��+2NaOH
CaO+CO2�� Ca��OH��2+Na2CO3��CaCO3��+2NaOH
��������
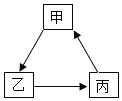
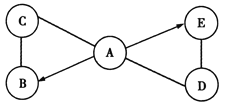
̼��Ƹ����������������ƣ�����A���Ͷ�����̼������B���������ƺ�ˮ��Ӧ�����������ƣ�����C�����������ƺ�̼���Ʒ�Ӧ����̼��ƣ�����D�����������ƣ���ҺE����
��1������C�Ļ�ѧʽ�� Ca��OH��2���ڲ������Ҫ���еķ������ʵ�ֵ��ǹ����Һ��ķ��룬Ϊ���ˡ�
��2���������̼����ڸ��������������ƺͶ�����̼����Ӧ�Ļ�ѧ����ʽ��CaCO3![]() CaO+CO2����
CaO+CO2����
��3����������������ƺ�̼���Ʒ�Ӧ����̼��Ƴ������������ƣ���Ӧ�Ļ�ѧ����ʽ��Ca��OH��2+Na2CO3��CaCO3��+2NaOH��

 Сѧ��ĩ���Ծ�ϵ�д�
Сѧ��ĩ���Ծ�ϵ�д�����Ŀ����ҵ���������·�Ӧ�ϳ�SO3��2SO2+O2![]() 2SO3��һ�������£���һ�ܱ�������Ͷ��SO2��O2��SO3��V2O5�������ʣ��ڲ�ͬʱ�̲�ø����ʵ���������λΪ�ˣ����±���ʾ������˵������ȷ���ǣ�������
2SO3��һ�������£���һ�ܱ�������Ͷ��SO2��O2��SO3��V2O5�������ʣ��ڲ�ͬʱ�̲�ø����ʵ���������λΪ�ˣ����±���ʾ������˵������ȷ���ǣ�������
�� | �� | �� | �� | |
t1 | 100 | 5 | 80 | 5 |
t2 | 60 | 55 | a | b |
t3 | 40 | c | d | 5 |
A. ������һ���Ǵ���V2O5
B. �μӷ�Ӧ��SO2���ӡ�O2���ӵĸ�����Ϊ2��1
C. ��������O2
D. d=15