题目内容
【题目】图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管(不考虑溶剂的蒸发),根据图象和有关信息判断,下列说法中错误的是( )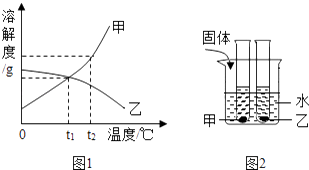
A.t2℃时,甲、乙两种物质的饱和溶液中溶质的质量分数大小关系为甲>乙
B.将甲、乙两种物质的饱和溶液都从t2℃将至t1℃时,两种溶液中溶质的质量分数相等
C.向烧杯的水中加NaOH固体后,只有乙溶液中溶质的质量分数变小
D.向烧杯的水中加NH4NO3固体后,只有盛放甲溶液的试管中有晶体析出
【答案】B
【解析】A、t2℃时甲的溶解度大于乙的溶解度,饱和溶液中溶质的质量分数= ![]() ×100%,则此时两物质的饱和溶液溶解度大的其饱和溶液的溶质质量分数大,则甲的溶质质量分数大于乙的溶质质量分数,A不符合题意;
×100%,则此时两物质的饱和溶液溶解度大的其饱和溶液的溶质质量分数大,则甲的溶质质量分数大于乙的溶质质量分数,A不符合题意;
B、甲的溶解度随温度的降低而减小,乙的溶解度随温度的降低而增大,将甲、乙两种物质的饱和溶液都从t2℃将至t1℃时,甲析出晶体,乙的溶解度变大则继续溶解试管内的固体,但溶解固体后是否饱和无法确定,若恰好饱和,则二者的溶质质量分数相等,若溶解后不饱和,则降温后甲的溶质质量分数大于乙的溶质质量分数,故降温后二者的溶质质量分数不一定相等,B符合题意;
C、氢氧化钠固体溶于水放出大量的热使溶液温度升高,甲物质逐步溶解,溶质的质量分数变大,乙的溶解度减小,析出晶体,溶质质量减小,溶剂不变,所以溶质的质量分数减小,C不符合题意;
D、NH4NO3固体溶于水吸收热量使溶液温度降低,甲的溶解度随温度的降低而减小,析出晶体,乙的溶解度随温度的升高而增大,变为不饱和溶液,不会析出晶体,D不符合题意.
故选:B.
A、t2℃时甲的溶解度大于乙的溶解度,饱和溶液中溶质的质量分数= 溶 解 度 溶 解 度 + 100 g ×100%,则此时两物质的饱和溶液溶解度大的其饱和溶液的溶质质量分数大;
B、甲的溶解度随温度的降低而减小,乙的溶解度随温度的降低而增大,并结合饱和溶液中溶质的质量分数= ![]() ×100%分析解答;
×100%分析解答;
C、氢氧化钠固体溶于水放出大量的热使溶液温度升高,结合二者溶解度随温度变化分析解答;
D、NH4NO3固体溶于水吸收热量使溶液温度降低,结合物质溶解度随温度变化分析解答.

