题目内容
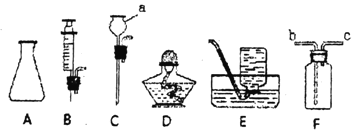
【题目】某校化学兴趣小组的同学对实验室制取氧气和氧气的某些性质进行了如下探究。已知图甲、图丁中装置的气密性良好。
(实验探究1)利用图甲所示装置探究影响H2O2分解速率的因素,装置中产生氧气的量可以用压强传感器测出(在等温条件下,产生氧气体积与装置内压强成正比,反应放热忽略不计),得到图乙所示的图像。
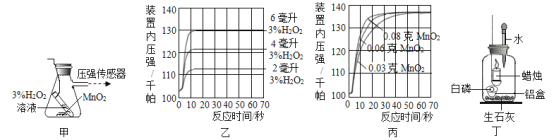
(1)写出图甲装置中发生反应的化学方程式:________。
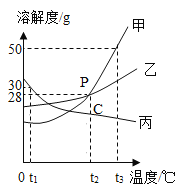
(2)图乙是“0.1克MnO2与不同体积的3%的H2O2溶液混合”的实验结果,从图中可以看出的规律是____________。
(3)图丙是用“8mL浓度为3%的H2O2溶液与不同质量的MnO2混合”时,所得到的曲线,通过该曲线可以得到的结论是_________。
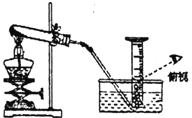
(实验探究2])利用图丁装置探究氧气的浓度对燃烧的影响。点燃蜡烛后立即塞紧橡皮塞,待蜡烛熄灭后,将滴管中的水全部滴入瓶中,铝盒中的白磷燃烧。
(1)白磷燃烧的主要现象是__________。
(2)由“蜡烛熄灭,白磷燃烧”可得出的结论是______。
(3)滴入水后白磷燃烧的原因是_________。
【答案】2H2O2![]() 2H2O+O2↑ 过氧化氢溶液越多,产生氧气越多 在过氧化氢溶液的质量与浓度相同的条件下,二氧化锰的质量越大,生成氧气的速率越快 产生白烟、放出热量 蜡烛熄灭后,集气瓶中仍然含有氧气 与水反应放热,引燃白磷
2H2O+O2↑ 过氧化氢溶液越多,产生氧气越多 在过氧化氢溶液的质量与浓度相同的条件下,二氧化锰的质量越大,生成氧气的速率越快 产生白烟、放出热量 蜡烛熄灭后,集气瓶中仍然含有氧气 与水反应放热,引燃白磷
【解析】
[实验探究1](1)装置甲中过氧化氢在二氧化锰的催化作用下反应生成水和氧气,发生反应的化学方程式为:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(2)图1乙是“0.1gMnO2与不同体积的3%H2O2溶液混合”的实验结果,从图中可以看出过氧化氢溶液越多,产生氧气越多;
(3)图丙是用“8mL浓度为3%的H2O2溶液与不同质量的MnO2混合”时,所得到的曲线,通过该曲线可知,在过氧化氢溶液的质量与浓度相同的条件下,二氧化锰的质量越大,生成氧气的速率越快;
[实验探究2](1)白磷燃烧,放出热量的同时产生了白烟;
(2)蜡烛熄灭后,白磷仍然能够在集气瓶中燃烧,说明蜡烛熄灭后,集气瓶中仍然含有氧气;
(3)在该实验中,生石灰的主要作用是:生石灰与水反应放出大量的热,温度达到了白磷的着火点,引燃白磷。

【题目】某化学兴趣小组,为了比较金属R与铁、铜的金属活动性强弱,进行如下探究活动:
(查阅资料)铁的活动性比铜强。
(进行猜想)对三种金属的活动性顺序作出如下猜想:
猜想一:R>Fe>Cu;
猜想二:_______;
猜想三:Fe>Cu>R。
(收集证据)为了验证哪一种猜想成立,甲、乙、丙三位同学分别展开实验探究。
主要操作 | 主要现象 | 实验结论 | |
甲 | 将打磨好的R丝插入盛有硫酸铜溶液的试管中 | ____________ | 猜想一正确 |
乙 | 将粗细相同打磨好的R丝、铁丝,分别插入体积和溶质质量分数都相同的稀盐酸中 | R丝表面产生气泡速率比铁丝表面产生气泡速率_____(填“快”或“慢”) | |
丙 | 将粗细相同打磨好的R丝、铁丝,分别在空气中点燃 | R丝在空气中剧烈燃烧,铁丝在空气中____ |
写出铁丝在氧气中燃烧的化学方程式________。
(交流反思)三位同学交流讨论后认为,比较金属活动性强弱的方法有多种。
(归纳总结)他们总结得出比较金属活动性强弱的常见方法有_______(填序号)
(1)金属与氧气反应的难易和剧烈程度;
(2)金属与酸溶液是否反应或反应的剧烈程度;
(3)金属与金属化合物溶液(盐溶液)是否反应。
【题目】在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如表所示,下列说法不正确的是( )
物质 | X | Y | Z | W |
反应前质量/g | 10 | 3 | 90 | 0 |
反应后质量/g | 3.2 | 3 | 待测 | 3.2 |
A. W可能是单质 B. Y可能是催化剂
C. 该反应是分解反应 D. 反应后Z物质的质量为![]()