题目内容
某化学小组的同学用下图所示装置做了两个兴趣实验。 
(1)检验装置Ⅰ气密性的方法是:关闭K1和K2,向长颈漏斗中注液体至液面高出漏斗的下端管口,静置片刻, ,即可证明装置不漏气。
(2)若关闭K1、K3,打开K2,装置Ⅳ可以收集到一种能使带火星的木条复燃的气体。装置Ⅰ中反应的化学方程式为 。
(3)若打开K1、K3,关闭K2,装置Ⅰ和装置Ⅲ中可得到两种不同的气体,此时在装置Ⅱ中可以观察到的现象是 。若装置Ⅰ中得到的气体不同于(2)中的气体,装置Ⅳ中收集到的气体可使紫色的石蕊溶液变红,装置Ⅰ中的固体物质可能是 ,装置Ⅲ中发生反应的化学方程式是 。
(1)继续加入液体,液面不再下降 (2)2H2O2  2H2O + O2↑
2H2O + O2↑
(3)装置II内的液面下降,导管中液面升高,盐酸流向装置III (2分)
氢前金属(锌、铁、镁等);CaCO3 +2HCl =CaCl2+ H2O + CO2↑
解析试题分析:(1)检查装置的气密性,就是检查装置是不是密闭的、不漏气,其检查原理是通过气体的发生装置与辅助容器中的液体(一般是水)构成一个密闭装置,依据改变密闭装置内压强时产生的现象(如冒气泡、形成水柱、液面的升降等)来判断其气密性的好坏,由于装置Ⅰ有2个出口,故要先设法堵住一个,再进行检查其气密性的好坏,即关闭K1和K2,然后再向长颈漏斗中注液体至液面高出漏斗的下端管口(形成密闭装置),静置片刻,若继续加入液体,液面不再下降,即可证明装置不漏气。
(2)由于关闭K1、K3,打开K2,装置Ⅳ可以收集到一种能使带火星的木条复燃的气体,即为氧气,故装置Ⅰ中的反应是过氧化氢的分解,故反应的化学方程式为2H2O2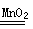 2H2O+O2↑。
2H2O+O2↑。
(3)若打开K1、K3,关闭K2,由于装置Ⅰ中产生了大量的气体并进入装置Ⅱ,故装置Ⅱ中压强增大,在气体的压力下,装置Ⅱ内的液面下降,导管中液面升高,盐酸流向装置Ⅲ;
若装置Ⅰ中得到的气体不同于(2)中的气体,那就是除了氧气之外的其它气体,结合气体的发生装置(固液不加热)可知,应为氢气或二氧化碳等气体;结合题意,装置Ⅳ中收集到的气体可使紫色的石蕊溶液变红,可知该气体应为CO2,则装置Ⅲ中发生反应的化学方程式为CaCO3 +2HCl =CaCl2+ H2O + CO2↑;则装置Ⅰ中得到的气体应为氢气,所以装置Ⅰ中的固体物质可能是锌、铁、镁等氢前金属。
考点:检查装置的气密性,二氧化碳的实验室制法,氧气的实验室制法,氢气的实验室制法,书写化学方程式
点评:化学是一门以实验为基础的学科,理解和熟练掌握装置的气密性检查的方法,以及常见气体的实验室制法,是解答本题的关键。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 某化学小组的同学用如图所示装置做了两个兴趣实验.
某化学小组的同学用如图所示装置做了两个兴趣实验.

