题目内容
【题目】稀硫酸、硫酸铜溶液、氢氧化钠溶液、铁钉是常见的四种物质,物质之间的反应关系如图所示。图中两圆相交部分(Ⅰ、Ⅱ、Ⅲ、Ⅳ)表示物质间两两反应。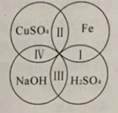
(1)基本反应类型中的反应。
(2)Ⅱ处反应现象是溶液由蓝色变成浅绿色,铁钉表面。
(3)Ⅲ处两种溶液反应,滴入酚酞试液后溶液变红,说明此溶液呈性。
(4)Ⅳ处反应的化学方程式是:。
【答案】
(1)置换
(2)有红色固体析出
(3)碱
(4)CuSO4+NaOH=Cu(OH)2↓+NaOH
【解析】解:(1)Ⅰ处是铁与稀硫酸反应生成硫酸盐铁和氢气,由一种单质跟一种化合物起反应,生成另一种单质和另一种化合物的反应叫做置换反应,Ⅰ处反应符合置换反应的特点,属于置换反应;(2)Ⅱ处是铁与硫酸铜溶液反应生成硫酸亚铁和铜,铜是红色固体,所以看到铁钉表面有红色固体析出;(3)Ⅲ处两种溶液反应,滴入酚酞试液后溶液变红,能使无色酚酞溶液变红的是碱性溶液;(4)Ⅳ处是硫酸铜与氢氧化钠反应生成氢氧化铜沉淀与硫酸钠,化学方程式为:CuSO4+NaOH=Cu(OH)2↓+NaOH。
所以答案是:(1)置换反应;(2)有红色固体析出;(3)碱;(4)CuSO4+NaOH=Cu(OH)2↓+NaOH。
【考点精析】根据题目的已知条件,利用金属活动性顺序及其应用和书写化学方程式、文字表达式、电离方程式的相关知识可以得到问题的答案,需要掌握在金属活动性顺序里:1、金属的位置越靠前,它的活动性就越强2、位于氢前面的金属能置换出盐酸、稀硫酸中的氢(不可用浓硫酸、硝酸)3、位于前面的金属能把位于后面的金属从它们的盐溶液中置换出来.(除K、Ca、Na);注意:a、配平 b、条件 c、箭号.

练习册系列答案
 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案
相关题目
