题目内容
【题目】空气中氧气含量测定的再认识。
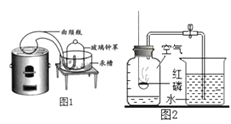

(经典赏析)教材中介绍了拉瓦锡用定量的方法研究了空气的成分(装置如图1),通过该实验拉瓦锡得出了氧气约占空气体积______的结论.
(实验回顾)(1)实验室常用红磷燃烧的方法测定空气中氧气的含量(装置如图2),兴趣小组用该方法测出的氧气含量常常远低于1/5。其原因可能是_____________;
(2)由于红磷在空气中点燃后才放入集气瓶内,实验缺陷:①测定结果不准确;②____。③_______
(提出问题)能否设计一套实验装置以解决上述缺陷?
(实验改进)
改进一:兴趣小组同学,设计了如图3所示装置
(查阅资料)白磷的着火点40℃,
(实验准备)锥形瓶内空气体积为230mL,注射器中水的体积为50mL,该装型气密性良好
(实验探究)装入药品,按图所示连接好仪器,夹紧弹资夹。先将锥形瓶底部放入热水中,白磷很快被引燃,然后将锥形瓶从热水中取出
(现象分析)
(1)锥形瓶底部放入热水中,白磷被引燃。
(2)整个实验过程中,气球的变化是_______。
(3)待白磷熄灭、锥形瓶冷却到室温后,打开弹簧夹,还可观察到的现象一是:注射器中的水自动喷射出来,原因是 __________现象二是:当注射中的水还剩约________ mL时停止流下。
改进二:兴趣小组同学又进行了大改进,设计图4和图5的实验方案。
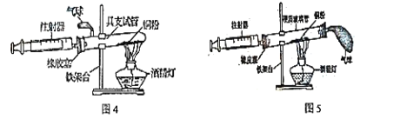
兴趣小组同学经过讨论认为图5的装置更合理,理由是___________。
兴趣小组同学按照图5装配好仪器,在给足量的铜粉加热时,实验中要来回推拉注射器,其目的是______,兴趣小组同学收到了良好的效果。
【答案】![]() 红磷的量不足或未冷却到室温就打开止水夹读数或装置漏气 燃烧产物污染空气 红磷点燃时,需打开装置,容易造成装置漏气 先变大,后缩小 白磷燃烧消耗了氧气,瓶内压强减小并小于外界大气压 4mL 能减小玻璃管内外的压强差,防止橡胶塞弹出 使铜与空气中的氧气充分接触
红磷的量不足或未冷却到室温就打开止水夹读数或装置漏气 燃烧产物污染空气 红磷点燃时,需打开装置,容易造成装置漏气 先变大,后缩小 白磷燃烧消耗了氧气,瓶内压强减小并小于外界大气压 4mL 能减小玻璃管内外的压强差,防止橡胶塞弹出 使铜与空气中的氧气充分接触
【解析】
经典赏析:通过实验拉瓦锡得出了氧气约占空气体积![]() 的结论。
的结论。
实验回顾:(1)用红磷燃烧的方法测定空气中氧气的含量,测出的氧气含量常常远低于![]() ,可能是红磷的量不足消耗了部分氧气或装置未冷却到室温就打开止水夹读数或装置漏气。(2)实验缺陷:测定结果不准确、燃烧产物污染空气、红磷点燃时,需打开装置,容易造成装置漏气。
,可能是红磷的量不足消耗了部分氧气或装置未冷却到室温就打开止水夹读数或装置漏气。(2)实验缺陷:测定结果不准确、燃烧产物污染空气、红磷点燃时,需打开装置,容易造成装置漏气。
现象(2)白磷燃烧放热,使瓶内压强增大,此时气球变大,而白磷燃烧消耗了氧气,冷却到室温后,瓶内压强减小,此时气球缩小,因此气球的变化是先变大,后缩小。(3)白磷燃烧消耗了氧气,瓶内压强减小并小于外界大气压,会使注射器中的水在外界大气压的作用下自动喷出来,由于空气中氧气的体积分数约占空气体积的![]() ,已知锥形瓶内空气体积为230mL,所以消耗的氧气的体积约为46mL,注射器中水的体积为50mL,其中46mL进入瓶中补充被消耗的氧气的体积,因此当注射器中的水还剩下约4mL时停止流下。
,已知锥形瓶内空气体积为230mL,所以消耗的氧气的体积约为46mL,注射器中水的体积为50mL,其中46mL进入瓶中补充被消耗的氧气的体积,因此当注射器中的水还剩下约4mL时停止流下。
改进二:图5的装置更合理,原因是能减小玻璃管内外的压强差,防止橡胶塞弹出。在给足量的铜粉加热时,实验中要来回推拉注射器,其目的是使空气中的氧气与铜充分接触。