题目内容
【题目】试依据核电荷数为1-18的元素的原子结构示意图,回答下列问题:
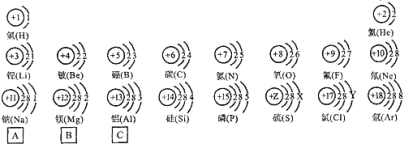
(1)现以第三周期(第11-18号元素)为例,仔细观察,从原子结构示意图分析,11~18号元素排在一行的依据是____________________;
(2)上图中硫元素的核电荷数Z=___________;氯元素的最外层电子数Y=___________(填数值);
(3)核电荷数为12的元素的原子失去两个电子后,形成的粒子的符号是___________;
(4)钙元素是人体中的常量元素,它在人体内99%存在于骨骼和牙齿中。该元素的原子结构示意图如图所示![]() ,则该元素的原子序数为___________,该元素属于___________(填“金属”或“非金属”)元素,该元素在上表中位于_________(选A.B.C)处。
,则该元素的原子序数为___________,该元素属于___________(填“金属”或“非金属”)元素,该元素在上表中位于_________(选A.B.C)处。
【答案】(1)都有三个电子层(2)16;7
(3)Mg2+(4)20;金属;B
【解析】
试题分析:在元素周期表中,电子层数等于周期数,从原子结构示意图分析,11~18号元素排在一行的依据是电子层数相同,都是三个电子层。核电荷数为12的元素是镁元素,失去两个电子后,形成带两个单位正电荷的阳离子,符号是Mg2+,在原子结构示意图中,圆圈内的数字为质子数;同一原子中,质子数=核外电子数=核电荷数=原子序数;最外层电子数小于4时,原子易失电子成为阳离子这类原子为金属元素,该微粒有四个电子层,在元素周期表中在第四周期。最外层电子数为2,排在第二列。所以位置为B

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目