题目内容
氢氧化钠固体暴露在空气中易变质,这是由于
2NaOH+CO2=Na2CO3+H2O
2NaOH+CO2=Na2CO3+H2O
(用化学方程式表示),实验室现有一瓶氢氧化钠固体,要检验其是否已变质,可取少量固体于试管中,然后加入盐酸
盐酸
来检验.分析:固体氢氧化钠在空气中易潮解,且氢氧化钠在空气中能吸收空气中的二氧化碳变质.
解答:解:氢氧化钠极易吸收水分而潮解并和空气中的二氧化碳反应生成碳酸钠和水而变质,最终生成碳酸钠.在实验室检验碳酸盐的存在常向样品中加盐酸,看是否会生成气体而进行检验.
故答案为:Na2CO3+2HCl=2NaCl+H2O+CO2↑;盐酸.
故答案为:Na2CO3+2HCl=2NaCl+H2O+CO2↑;盐酸.
点评:氢氧化钠在空气中易潮解且易吸收空气中的二氧化碳,所以氢氧化钠在空气中易变质,所以氢氧化钠要密封保存.

练习册系列答案
相关题目
 17、某兴趣小组的同学在学习完酸碱盐的性质后进入实验室进行实验.小明在实验中却看到了一个不和谐的“音符”(如右图).
17、某兴趣小组的同学在学习完酸碱盐的性质后进入实验室进行实验.小明在实验中却看到了一个不和谐的“音符”(如右图).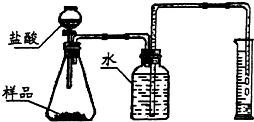 某兴趣小组对氢氧化钠固体暴露在空气中的变质情况进行了研究.把一小块固体氢氧化钠放在表面皿里,长时间暴露在空气中,发现其固体表面逐渐湿润,部分熔化成液体后又逐渐形成晶体,最终变成粉末.请回答兴趣小组产生的下列问题:
某兴趣小组对氢氧化钠固体暴露在空气中的变质情况进行了研究.把一小块固体氢氧化钠放在表面皿里,长时间暴露在空气中,发现其固体表面逐渐湿润,部分熔化成液体后又逐渐形成晶体,最终变成粉末.请回答兴趣小组产生的下列问题: