题目内容
【题目】在图中的烧杯中盛有65℃的热水,杯底放有一小粒足够量的白磷,然后将一支有刻度的空试管垂直插入烧杯中,试管口罩住白磷。(已知白磷熔点 44℃,着火点为 40℃)。
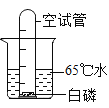
(1)写出实验过程中发生的现象_。
(2)该实验说明了_。
【答案】试管口罩住的白磷燃烧,产生大量的白烟,热水进入试管,进入热水的体积约占试管容积的五分之一。 可燃物要燃烧除了温度达到着火点外,还需与氧气接触;同时还证明了空气中氧气含量约占空气体积的五分之一。
【解析】
(1)实验过程中,当用空试管垂直插入烧杯中,试管口罩住白磷时,白磷燃烧,产生大量的白烟,热水进入试管,进入热水的体积约占试管容积的五分之一。
(2)当用空试管垂直插入烧杯中,试管口罩住白磷,使白磷与空气接触,白磷燃烧,说明可燃物要燃烧除了温度达到着火点外,还需与氧气接触;反应停止后,由于消耗了氧气,压强减小,热水进入试管,氧气约占空气体积分数的1/5,故进入热水的体积约占试管容积的五分之一,说明空气中氧气的含量约占空气体积的五分之一。

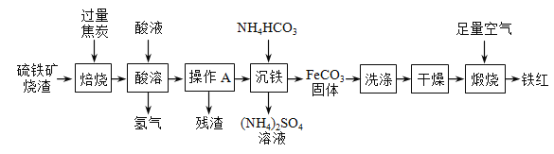
【题目】某化学兴趣小组为探究金属铝和铜的活动性强弱,开展了以下活动。
[查阅资料]经查阅,金属铝在常温下能与空气中的氧气反应生成致密的氧化铝薄膜。该反应的化学方程式为_________________。
[对比实验]
编号 | 操作 | 现象 |
甲 | 将表面未打磨的铝丝浸入CuSO4溶液中 | 无明显现象 |
乙 | 将表面打磨后的铝丝浸入CuSO4溶液中 | 铝丝表面析出红色固体 |
丙 | 将表面未打磨的铝丝浸入CuCl2溶液中 | 铝丝表面析出红色固体 |
(1)比较实验乙和实验_______________(填“甲”或“丙”)可得知:打磨能破坏氧化铝薄膜。
(2)小明同学对实验丙的现象进行分析,认为H2O对氧化铝薄膜有破坏作用。但此观点马上被其他同学否定,否定的依据是____________________。
[猜测与探究]
小组同学针对实验丙的现象,经讨论后猜测:Cl-破坏了氧化铝薄膜。
为检验此猜测是否正确,他们首先向两支试管中加入相同的CuSO4溶液,并均浸入表面未打磨的铝丝,然后进行了新的探究:
操作 | 现象 | 结论 | 推论 |
(1)向一支试管中再加入NaCl固体 | 铝丝表面析出红色固体 | 氧化铝薄膜被破坏 | Na+或___________能破坏氧化铝薄膜 |
(2)向另一支试管中再加入Na2SO4固体 | ___ | 氧化铝薄膜未被破坏 | Na+和SO42-都不能破坏氧化铝薄膜 |
[结论与反思]得出结论:前述猜测___(填“正确”或“不正确”)
[拓展应用]家庭里的铝制品在使用时要避免与______________接触(填一种即可)
总结反思:本次探究充分运用了比较法和控制变量法