题目内容
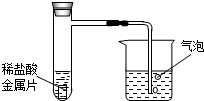 如图所示,某同学将甲、乙、丙三种大小和形状均相同的 金属片,分别放入相同体积、相同质量分数的稀盐酸中.观察反应开始时从导管口冒出的气泡并作如下记录:
如图所示,某同学将甲、乙、丙三种大小和形状均相同的 金属片,分别放入相同体积、相同质量分数的稀盐酸中.观察反应开始时从导管口冒出的气泡并作如下记录:
| 金属种类 | 甲 | 乙 | 丙 |
| 气泡多少 | 多 | 没有 | 少 |
- A.镁
- B.铁
- C.铜
- D.无法判断
C
分析:本题研究不同金属跟稀硫酸反应的情况,利用表格中的记录可判断是否产生氢气并得出金属的活泼性强弱,结合氢前的金属可与酸反应生成氢气,氢后金属不能与酸反应生成氢气解决.
解答:根据金属活动性顺序表可知镁、铁、铜、氢的活动性由强到弱依次是镁>铁>氢>铜,根据氢后金属不能与酸反应生成氢气可知,没有生成气体的只能是铜.
故选C
点评:本题以实验探究的方式利用金属与酸的反应的实验记录来考查金属活泼性,学生应结合金属活动性顺序表的意义并利用表格中的记录作出正确的判断.
分析:本题研究不同金属跟稀硫酸反应的情况,利用表格中的记录可判断是否产生氢气并得出金属的活泼性强弱,结合氢前的金属可与酸反应生成氢气,氢后金属不能与酸反应生成氢气解决.
解答:根据金属活动性顺序表可知镁、铁、铜、氢的活动性由强到弱依次是镁>铁>氢>铜,根据氢后金属不能与酸反应生成氢气可知,没有生成气体的只能是铜.
故选C
点评:本题以实验探究的方式利用金属与酸的反应的实验记录来考查金属活泼性,学生应结合金属活动性顺序表的意义并利用表格中的记录作出正确的判断.

练习册系列答案
相关题目
 14、如图所示,某同学将甲、乙、丙三种大小和形状均相同的 金属片,分别放入相同体积、相同质量分数的稀盐酸中.观察反应开始时从导管口冒出的气泡并作如下记录: 14、如图所示,某同学将甲、乙、丙三种大小和形状均相同的 金属片,分别放入相同体积、相同质量分数的稀盐酸中.观察反应开始时从导管口冒出的气泡并作如下记录:
|
如图所示,某同学将甲、乙、丙三种大小和形状均相同的 金属片,分别放入相同体积、相同质量分数的稀盐酸中.观察反应开始时从导管口冒出的气泡并作如下记录:
如果三种金属分别是镁、铁、铜中的一种,则乙可能是( )

A.镁
B.铁
C.铜
D.无法判断
| 金属种类 | 甲 | 乙 | 丙 |
| 气泡多少 | 多 | 没有 | 少 |

A.镁
B.铁
C.铜
D.无法判断
如图所示,某同学将甲、乙、丙三种大小和形状均相同的 金属片,分别放入相同体积、相同质量分数的稀盐酸中.观察反应开始时从导管口冒出的气泡并作如下记录:
如果三种金属分别是镁、铁、铜中的一种,则乙可能是( )

A.镁
B.铁
C.铜
D.无法判断
| 金属种类 | 甲 | 乙 | 丙 |
| 气泡多少 | 多 | 没有 | 少 |

A.镁
B.铁
C.铜
D.无法判断
如图所示,某同学将甲、乙、丙三种大小和形状均相同的 金属片,分别放入相同体积、相同质量分数的稀盐酸中.观察反应开始时从导管口冒出的气泡并作如下记录:
如果三种金属分别是镁、铁、铜中的一种,则乙可能是( )

A.镁
B.铁
C.铜
D.无法判断
| 金属种类 | 甲 | 乙 | 丙 |
| 气泡多少 | 多 | 没有 | 少 |

A.镁
B.铁
C.铜
D.无法判断
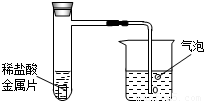
如图所示,某同学将甲、乙、丙三种大小和形状均相同的 金属片,分别放入相同体积、相同质量分数的稀盐酸中.观察反应开始时从导管口冒出的气泡并作如下记录:
如果三种金属分别是镁、铁、铜中的一种,则乙可能是( )
A.镁
B.铁
C.铜
D.无法判断
| 金属种类 | 甲 | 乙 | 丙 |
| 气泡多少 | 多 | 没有 | 少 |

A.镁
B.铁
C.铜
D.无法判断